题目内容
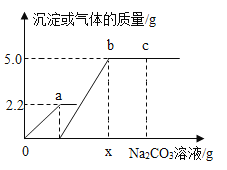
【题目】将10%的Na2CO3溶液逐滴加入CaCl2和HCl的混合溶液中,加入Na2CO3溶液的质量与产生沉淀或气体的质量关系如下图所示。下列说法正确的是
A. a点时溶液的pH大于c点时溶液的pH
B. b点时,溶液中有2种盐
C. x值为106.0
D. oa段是产生沉淀的反应
【答案】C
【解析】
碳酸钠与盐酸反应生成氯化钠、水和二氧化碳,碳酸钠与氯化钙反应生成碳酸钙沉淀和氯化钠;加入的碳酸钠先与盐酸反应,把盐酸消耗完了,才开始与氯化钙反应,开始生成沉淀。最后到达最高点说明已经完全反应。
A、a点时稀盐酸被完全消耗,此时溶液显中性;c点的溶液中含有Na2CO3、NaCl两种溶质,由于Na2CO3显碱性,NaCl显中性,c的溶液的pH>7;a点时溶液的pH小于c点时溶液的pH,故选项错误;
B、b点表示碳酸钠恰好完全反应,溶液中只含有NaCl一种溶质,故选项错误;
C、由图示可知碳酸钠与盐酸反应生成气体2.2g,碳酸钠与氯化钙反应生成沉淀5.0g。设生成2.2g气体所需的Na2CO3的质量为y,生成沉淀5.0g所需Na2CO3的质量为z
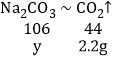
![]()
解得 y=5.3g
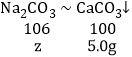
![]()
解得 z=5.3g
x值为(5.3g+5.3g)÷10%=106g,故选项正确;
D、图中oa段表示生成的气体质量,故选项错误。故选C。

练习册系列答案
相关题目