题目内容
下列实验方案或措施合理的是( )
| A、除去CaO中混有的CaCO3,先加足量水,然后过滤 | B、除去MnO2粉末中混有的KCl,先加足量水溶解、过滤、洗涤、干燥 | C、用无色酚酞试剂检测氢氧化钠是否变质 | D、用碘化钾检测食品中是否含有淀粉 |
考点:化学实验方案设计与评价,碱的化学性质,盐的化学性质,鉴别淀粉、葡萄糖的方法与蛋白质的性质
专题:简单实验方案的设计与评价
分析:A、除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
B、除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
C、根据氢氧化钠能与空气中的二氧化碳反应生成碳酸钠而变质,碳酸钠与氢氧化钠均显碱性,进行进行分析判断.
D、根据碘遇淀粉变蓝色进行分析判断.
B、除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
C、根据氢氧化钠能与空气中的二氧化碳反应生成碳酸钠而变质,碳酸钠与氢氧化钠均显碱性,进行进行分析判断.
D、根据碘遇淀粉变蓝色进行分析判断.
解答:解:A、氧化钙能与水反应生成氢氧化钙,碳酸钙难溶于水,反而会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
B、KCl易溶于水,MnO2粉末难溶于水,可采取加水溶解、过滤、洗涤、干燥的方法进行分离除杂,故选项所采取的方法正确.
C、碳酸钠和氢氧化钠均显碱性,均能使酚酞溶液变红色,不能选用无色酚酞试液判断氢氧化钠是否变质,故选项所采取的方法错误.
D、碘单质遇淀粉变蓝色,用碘化钾不能检测食品中是否含有淀粉,故选项所采取的方法错误.
故选:B.
B、KCl易溶于水,MnO2粉末难溶于水,可采取加水溶解、过滤、洗涤、干燥的方法进行分离除杂,故选项所采取的方法正确.
C、碳酸钠和氢氧化钠均显碱性,均能使酚酞溶液变红色,不能选用无色酚酞试液判断氢氧化钠是否变质,故选项所采取的方法错误.
D、碘单质遇淀粉变蓝色,用碘化钾不能检测食品中是否含有淀粉,故选项所采取的方法错误.
故选:B.
点评:本题难度不大,但综合性较强,化学实验方案的设计是考查学生能力的主要类型,同时也是实验教与学难点,在具体设计时要对其原理透彻理解,可根据物质的物理性质和化学性质结合实验目的进行分析判断.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列物质的用途主要与其化学性质相关的是( )
| A、液氨作医疗冷冻剂 | B、一氧化碳用于冶炼金属 | C、氢气用于充填气球 | D、用石墨作润滑剂 |
科学的假设与猜想是科学探究的先导和价值所在.在下列假设(猜想)引导下的探究肯定没有意义的选项是( )
| A、探究二氧化硫和水反应可能有硫酸生成 | B、探究铁制品表面红色的物质可能只是四氧化三铁 | C、探究铁与硫酸的反应产生的气体可能是氧气 | D、探究铜在灼烧时出现的黑色物质可能是炭黑 |
下列是对一些实验操作的设计或描述,其中错误的是( )
| A、有气体参加或生成的化学反应需要在密闭容器中进行才能验证其质量守恒 | B、实验室制备气体选择发生装置时,首先要考虑反应物的状态和反应条件 | C、测定未知溶液的酸碱度时,可以将pH试纸直接伸到待测溶液中 | D、检验久置于空气中的氢氧化钠溶液是否变质,可用氯化钡溶液进行验证 |
下列实验方案中,合理的是( )
| A、分离木炭粉和CuO:在空气中充分灼烧 | B、验证质量守恒定律:比较镁条燃烧前后固体质量 | C、制备Fe(OH)3:向FeCl3溶液中加入NaOH溶液,过滤、洗涤、干燥 | D、除去CO2中的HCl和水蒸气:依次通过过量的NaOH溶液、浓硫酸 |
下列实验不能达到实验目的是( )
A、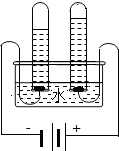 探究水的组成 | B、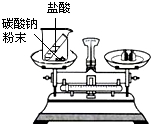 探究化学反应是否遵循质量守恒定律 | C、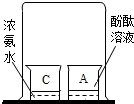 探究分子运动 | D、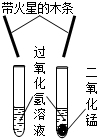 探究二氧化锰是否加快过氧化氢分解 |
下列实验方法中可行的是( )
| A、用活性炭软化硬水 | B、用向上排空气法收集氢气 | C、用石蕊溶液鉴别稀盐酸和稀硫酸 | D、用点燃闻气味的方法区别棉线和羊毛线 |
下列实验设计不能达到实验目的是( )
A、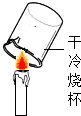 探究石蜡中含有氢元素 | B、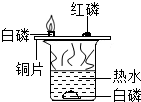 探究燃烧的条件 | C、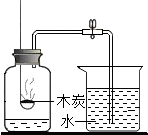 燃烧木炭测定空气中氧气的含量 | D、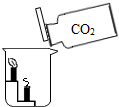 证明CO2密度比空气大 |
下列实验设计及操作,其现象足以说明结论的是( )
| A、将浓盐酸和大理石反应放出的气体通入石灰水,始终未浑浊,则石灰水一定变质 | B、取某氢氧化钠溶液放入试管中,滴加一定量的稀盐酸,没有气泡冒出,则氢氧化钠一定没有变质 | C、向滴有酚酞的稀氢氧化钠溶液的试管中滴加稀盐酸,红色褪去,则说明二者发生反应 | D、将充满二氧化碳气体的试管倒扣在盛有氢氧化钠溶液的水槽中,试管内液面上升,则说明二氧化碳与氢氧化钠一定发生了反应 |