题目内容
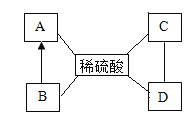
【题目】归纳是学习的重要方法。学完盐的性质后,小郑归纳出酸的 A、B、C、D、E 五条化学性质,并用“五角星”呈现出来,见下图:
(1)图中酸的 D 性质中,即“五角星”右下角里面对应物质的类别是____________;

(2)紫色石蕊试液滴入酸中,溶液显_____________色;
(3)若酸是硫酸,请写出用稀硫酸清除铁锈的主要反 应化学方程式:________________;
(4)若酸是盐酸,请你选择一种常见的物质来检验酸 的 D 性质___________________(填化学式);
(5)小郑探究 Mg 和 Fe 与酸液反应的快慢,需要控制的变量是______________________(填代号)。
①金属的聚集形态(形状);②酸液起始温度;③酸液种类;④酸液的浓度;⑤反应容器的大小
【答案】盐 红 Fe2O3 + 3H2SO4 = Fe2(SO4)3 + 3H2O AgNO3 (或 Na2CO3 等) ①②③④
【解析】
(1)酸的化学性质:酸溶液能跟酸碱指示剂起反应、酸能跟多种活泼金属起反应、酸能跟金属氧化物反应生成盐和水、酸能跟碱起中和反应生成盐和水、酸能跟某些盐反应生成另一种酸和另一种盐。图中酸的 D 性质中,即“五角星”右下角里面对应物质的类别是盐;
(2)石蕊遇酸性溶液会变红色,所以将紫色石蕊试液滴加到酸溶液中溶液变红;
(3)硫酸与氧化铁反应生成硫酸铁和水,反应的化学方程式为:Fe2O3 + 3H2SO4 = Fe2(SO4)3 + 3H2O;
(4)盐酸与硝酸银反应生成氯化银的白色沉淀和硝酸,盐酸与碳酸钠反应生成氯化钠、水和二氧化碳。若酸是盐酸,可选择AgNO3 (或 Na2CO3 等)来检验酸 D 性质;
(5)影响化学反应速率的因素有:反应物本身的性质、温度、反应物浓度、反应物之间的接触面积等。控制变量法要创设相同的外部条件,探究镁和锌与盐酸反应的快慢,需要控制不变的条件就是对反应速度可能有影响的因素,分析可知五个因素中只有容器的大小对反应速度无影响,需要控制的变量是①②③④。

 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案【题目】如表是国家对“饮酒驾车”和“醉酒驾车”的界定标准。
饮酒驾车 | 20mg/100mL≤血液中的酒精含量<80mg/100mL |
醉酒驾车 | 血液中的酒精含量≥80mg/100mL |
(1)乙醇分子中碳、氢、氧各原子个数比为_____,其中碳、氢元素的质量比是_____。
(2)乙醇中碳元素的质量分数为_____。(结果精确到0.1%)。
(3)饮酒会使人的神经系统过渡兴奋或麻痹抑制,容易引发交通事故。某人饮酒后驾车,被交警发现,经测定其每10mL血液中酒精含量为9.3mg,属于_____驾车。
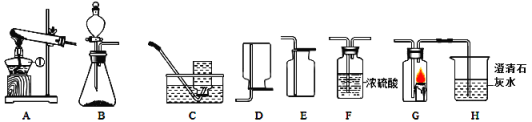
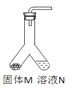
【题目】表中的装置制取气体(制取时将装置中的固体与液体混合)。下表为气体的制取的装置和反应的化学方程式
制取气体的装置 | 固体M | 溶液N | 制取的气体 | 反应的化学方程式 |
| 大理石 | _______。 | CO2 | __________; |
锌粒 | 稀硫酸 | ________; | __________; |