题目内容
【题目】如表是国家对“饮酒驾车”和“醉酒驾车”的界定标准。
饮酒驾车 | 20mg/100mL≤血液中的酒精含量<80mg/100mL |
醉酒驾车 | 血液中的酒精含量≥80mg/100mL |
(1)乙醇分子中碳、氢、氧各原子个数比为_____,其中碳、氢元素的质量比是_____。
(2)乙醇中碳元素的质量分数为_____。(结果精确到0.1%)。
(3)饮酒会使人的神经系统过渡兴奋或麻痹抑制,容易引发交通事故。某人饮酒后驾车,被交警发现,经测定其每10mL血液中酒精含量为9.3mg,属于_____驾车。
【答案】2∶6∶1 4∶1 52.2% 醉酒
【解析】
(1)由化学式可知,乙醇分子中碳、氢、氧各原子个数比为2:6:1;其中碳、氢元素的质量比是(12×2):(1×6)=4:1;故填:2:6:1;4:1;
(2)乙醇中碳元素的质量分数为![]() ,故填:52.2%;
,故填:52.2%;
(3)由表格信息可知,血液中的酒精含量≥80毫克/100毫升,因此经测定其每10毫升血液中酒精含量为9.3毫克,即每100毫升血液中酒精含量为93毫克,属于醉酒驾车;故填:醉酒。

【题目】某化学学习兴趣小组为了测定某生理盐水的溶质质量分数,实验过程和有关实验数据如图所示:

根据上图信息解决下列问题:
(1)已知过滤后获得的固体物质是一种纯净物,则该物质的名称是____________,质量是__________g。
(2)该生理盐水的溶质质量分数是多少?(写出运算过程)________________
(3)请在图上作出往生理盐水滴加 AgNO3 溶液, 产生 AgCl 沉淀的质量与参与反应的 AgNO3 溶液的质量之间的关系图像。__________
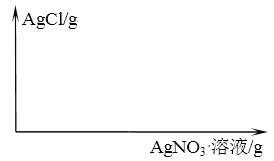
(4)已知硝酸钠的溶解度如表所示,据此估算判断该实验获得的 161.13g 溶液在常温下属于___________________溶液(填“饱和”或“不饱和”)。
硝酸钠在水中的溶解度
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
溶解度/g | 73 | 80 | 87 | 98 | 103 | 113 | 124 | 137 | 150 | 163 | 180 |
【题目】Mg(OH)2 被添加于塑料、橡胶等易燃物中,在受热分解时吸收热量并释放出水而起到阻燃作用,同时生成的氧化镁,化学性质稳定,不产生二次污染。
(1)写出Mg(OH)2 受热分解反应的化学方程式:_________________。
(2)实验室模拟制取Mg(OH)2 的一个实验是:一定温度下,往一定量氯化镁中加入氨水,生成Mg(OH)2 沉淀,再通过结晶、过滤,得到Mg(OH)2 晶体。为探究获得较高Mg(OH)2晶体转化率的条件,某研究小组进行下述对比实验,数据如下表:
实验 | 结晶温度/℃ | 结晶时间/min | 转化率/% |
a | 20 | 30 | 53.15 |
b | 40 | 30 | 84.12 |
c | 40 | 45 | 63.00 |
d | 60 | 60 | 62.20 |
①该小组研究的结晶条件是_____和_____。
②实验_____和_______(填序号)说明在其它条件相同的情况下,结晶时间相同时,温度越高,Mg(OH)2 转化率越高。
③实验b和c的目的是____。
④在上述四组实验中,最佳的结晶条件是____℃和_____min。