题目内容
【题目】下图是木炭还原氧化铜的探究实验装置。
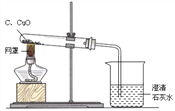
【提出问题】木炭还原氧化铜产生什么气体?
【提出猜想】产生的气体有三种情况:⑴CO,⑵CO2, ⑶ ______________。
【设计方案】实验前后分别对试管和烧杯里的物质进行称量,数据设计如下:
称量对象 | 反应前质量 | 反应后质量 | 质量差 |
试管+固体混合物 | M1 | M2 | △m1即( M1-M2) |
烧杯+澄清石灰水 | M3 | M4 | △m2即( M4-M3) |
(1)若△m2=0,说明反应产生的气体不能被澄清石灰水吸收,则猜想__________成立。
(2)若猜想②正确,理论上△m1与△m2 的关系是:△m1______△m2(填“>”、“<”或“=”)。
【实验并记录】实验得到的数据如下表:
称量对象 | 反应前质量 | 反应后质量 | 质量差 |
试管+固体混合物 | 69.8g | 65.4g | △m1 |
烧杯+澄清石灰水 | 118.8g | 122.6g | △m2 |
用以上实验数据分析,结果应该是猜想________成立。
【反思与评价】经查阅资料知道:木炭还原氧化铜产生CO2气体,该反应的化学方程式为:_____。本次实验结果与资料显示不一致。对其可能原因有同学提出下列分析,其中合理的是__________。
A.装置漏气 B.生成的CO2部分与过量的C反应生成了CO
C.澄清石灰水吸收CO2效果不好 D.装置内还有CO2气体未被吸收
【答案】 CO和CO2 ﹙1﹚ = 猜想(3)成立 C+2CuO![]() 2Cu+ CO2↑ ABCD
2Cu+ CO2↑ ABCD
【解析】【提出猜想】产生的气体是CO和CO2的混合气体。【设计方案】(1)若△m2=0,说明反应产生的气体不能被澄清石灰水吸收,则产生的气体不是二氧化碳,猜想⑴成立。(2)△m2等于生成的二氧化碳的质量,如果产生的气体只有二氧化碳,根据质量守恒定律,△m1=△m2
【实验并记录】△m1=69.8g-65.4g=4.4g,△m2=122.6g-118.8g=3.8g,则猜想(3)成立。【反思与评价】木炭还原氧化铜的化学方程式为:C + 2CuO高温 2Cu + CO2↑。A.装置漏气,加热时会有一部分气体跑到空气中去了,正确;B.生成的CO2部分与过量的C反应生成了CO而跑到空气中去了,正确;C.澄清石灰水吸收CO2效果不好,有部分二氧化碳没被吸收跑到空气中去了,正确;D.装置内还有CO2气体未被吸收,使得△m2偏小,正确。故选ABCD。

 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案