题目内容
【题目】(1)化学实验室要从X、银、铜、锌四种金属混合物中分离某贵重金属。流程如下:
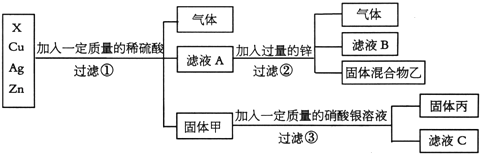
请回答:
①四种金属的活动性顺序由强到弱的是_________________;
②固体丙中一定含有的金属是__________________;
③写出③中反应的化学方程式_______________________;
④为了检验滤液C中的溶质成分:向其中加入稀盐酸,有白色沉淀产生,则滤液C中一定含有的阳离子___.
(2)配制50 g一定溶质质量分数的氯化钠溶液,实验步骤如下:

①计算:氯化钠质量和水的体积(水的密度:1.0 g/mL).
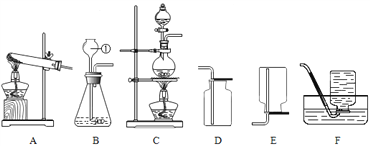
②称量:如上图1所示(右盘无砝码),称得的氯化钠质量为________g.
③溶解:把氯化钠和水全部转移到烧杯中,搅拌至氯化钠全部溶解,配得氯化钠溶液中溶质的质量分数为________(写出计算式和结果)。
④装瓶、贴标签。
⑤上述实验过程中,用量筒量取水时,若按上图2方式进行读数,将导致所配制溶液的溶质质量分数______(填“偏大”、“不变”或“偏小”)。
⑥若将上述50 g氯化钠溶液稀释为2%的氯化钠溶液,稀释过程中,不需要用到的仪器有______(填标号)。
A.量筒 B.漏斗 C.玻璃棒 D.托盘天平
【答案】 Zn﹥X﹥Cu﹥Ag Ag Cu+2AgNO3===2Ag+Cu(NO3)2 Ag+、Cu2+ 4.0 ![]() ×100% =8% 偏小 BD
×100% =8% 偏小 BD
【解析】(1)要从X、银、铜、锌四种金属混合物中分离某贵重金属。稀硫酸与铜和银均不反应,锌与硫酸反应生成硫酸锌和氢气,滤液A与过量锌反应生成固体混合物乙,x与硫酸反应,锌可以置换出x,锌比x活泼;固体甲是铜和银,铜比银活泼,铜与硝酸银溶液反应置换出银,固体丙是银。①四种金属的活动性顺序由强到弱的是Zn﹥X﹥Cu﹥Ag。②固体丙中一定含有的金属是Ag,四种金属中银最不活泼。③其中③中反应的化学方程式是Cu+2AgNO3==2Ag+Cu(NO3)2,铜比银活泼,铜可以把银从它的盐溶液中置换出来。④为了检验滤液C中的溶质成分:向其中加入稀盐酸,有白色沉淀产生,则滤液C中一定含有的阳离子是Ag+、Cu2+ ,氯化银白色沉淀,不溶于酸,Cu+2AgNO3=2Ag+Cu(NO3)2。(2)配制50 g一定溶质质量分数的氯化钠溶液。根据所学知识和题中信息知,①计算:氯化钠质量∶②称量:称得的氯化钠质量为4.0g。③溶解:把氯化钠和水全部转移到烧杯中,搅拌至氯化钠全部溶解,配得氯化钠溶液中溶质的质量分数为![]() ×100%=8%。④装瓶、贴标签。⑤用量筒量取水时,仰视读数,得到水多,将导致所配制溶液的溶质质量分数偏小。⑥将50g氯化钠溶液稀释为2%的氯化钠溶液,稀释过程中,不需要用到的仪器有漏斗和托盘天平。故选BD。
×100%=8%。④装瓶、贴标签。⑤用量筒量取水时,仰视读数,得到水多,将导致所配制溶液的溶质质量分数偏小。⑥将50g氯化钠溶液稀释为2%的氯化钠溶液,稀释过程中,不需要用到的仪器有漏斗和托盘天平。故选BD。
点睛∶量筒读数应平视。托盘天平应左物右码,读数应是砝码加上游码。浓溶液稀释成稀溶液需要量筒量取水,玻璃棒搅拌。

【题目】用下列实验操作可完成两个实验。请从A或B 两题中任选一个作答,若两题均作答,按A 计分。
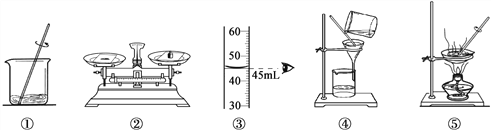
A去除粗盐中难溶性杂质 | B配制50g 10%的氯化钠溶液 |
(1)实验的操作步骤是___________(填序号)。 (2)实验中发现滤液浑浊,其原因是_____。 a.滤纸未贴紧漏斗内壁 b.滤纸破损 | (1)实验的操作步骤是____________(填序号)。 (2)实验后测得溶质质量分数<10%,其原因是_____。 a.装瓶时溶液洒出 b.烧杯中有水 |
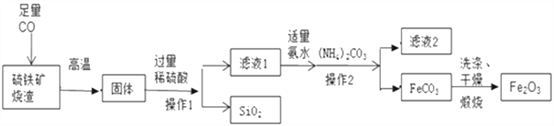
【题目】氧化铜矿石含有CuO、Cu2(OH)2CO3和Fe2O3,还含有一些不溶于水、不溶于酸的其他杂质。铜、铁是畜禽所必需的微量元素,某饲料厂联合生产硫酸铜晶体和硫酸亚铁晶体的主要工艺流程如下。
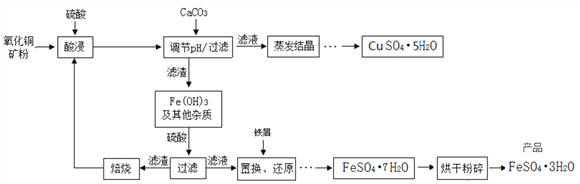
【资料】Cu2+、Fe3+以氢氧化物形式沉淀时溶液的pH见下表:
沉淀物 | Fe(OH)3 | Cu(OH)2 |
开始沉淀的pH | 1.5 | 4.2 |
沉淀完全的pH | 3.7 | 6.7 |
请回答问题:
(1)氧化铜矿石粉碎的目的是________________________________。
(2)写出“酸浸”中发生反应的化学方程式__________________(任写一个)。
(3)该流程中氢氧化铁能与硫酸反应,其基本反应类型是_________反应。
(4)下图为“硫酸亚铁干燥曲线图”,据此可确定由FeSO4·7H2O脱水得到流程中所示产品的适宜工艺条件为__________________(填写温度和时间)。
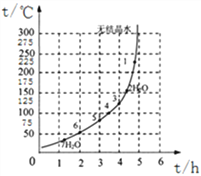
(5)在“调节pH/过滤”中,加入CaCO3调节溶液的pH,请说出溶液适宜的pH范围是____________。