题目内容
【题目】取10.9g纯碱样品(含少量氯化钠杂质)完全溶于108.8g水中,再向其中逐滴加入100g溶质质量分数为20.8%的氯化钡溶液,恰好完全反应,所得溶液为不饱和溶液,请根据题意回答下列问题:
(1)100g溶质质量分数为20.8%的氯化钡溶液中氯化钡的质量为__g;
(2)完全反应后所得溶液中溶质的质量分数为多少_______? (写出计算过程)。
【答案】 20.8 6%
【解析】本题主要考查运用化学方程式和溶质质量分数公式综合分析和解决实际问题的能力。
(1)氯化钡溶液中氯化钡的质量为:100g×20.8%=20.8g;
(2)设:纯碱样品中Na2CO3的质量为x,生成NaCl的质量为y,生成碳酸钡沉淀质量为z,
Na2CO3 +BaCl2=BaCO3↓+2NaCl
106 208 197 117
x 20.8g z y
![]() 解得:x=10.6g;
解得:x=10.6g;
![]() 解得:y=11.7g;
解得:y=11.7g;
![]() 解得:z=19.7g;
解得:z=19.7g;
完全反应后所得溶液中溶质的质量分数为:![]() ×100%=6%;
×100%=6%;
答:氯化钡溶液中氯化钡的质量为20.8g;
完全反应后所得溶液中溶质的质量分数为6%。

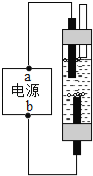
【题目】订书钉是生活中常用文具,顾老师指导同学们围绕订书们钉开展实验研究。
实验步骤 | 实验内容 |
① | 用磁铁吸引订书钉,发现订书钉能被吸引 |
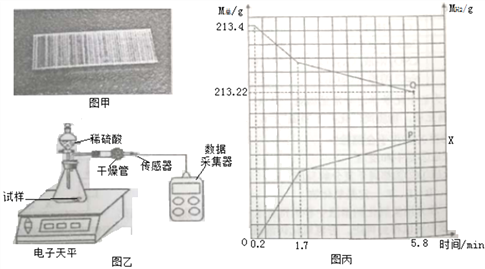
② | 取一个订书钉块(40根钉子)(如图甲所示),浸入酒精中,一段时间后能从订书钉块上取下一层胶水薄膜 |
③ | 取上述订书钉块用棉花擦去精,并待酒精完全挥发后称量其质量为13.4g |
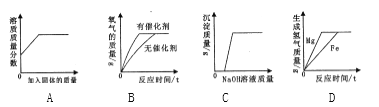
④ | 将其放入图乙所示装置,并在干管口用氢气传感器测量氢气质量,同时记录质量变化 (如图丙所示) |
⑤ | 5.8分钟时停止反应取出装置剩余订书钉,洗涤、干操、称量,剩余订书钉质量为7.8g |
问题思考:
(1)订书钉表面涂胶水的目的主要是_______________;
(2)查阅资料可知:订书钉主要成分为铁,并在其表面镀一种金属。请结合图丙分析:
①图丙中P点纵坐标X的值_______________________;
②0→0.2分钟不产生氢气的原因主要是______________;
③请写出1.7分钟后装置中发生的主要化学反应方程式____________;
④订书钉表面镀的金属可能是钙、镁、铝、锌、铜中的一种,请根据实验分析该金属是_______。