题目内容
【题目】根据信息写出下列化学方程式。
(1)人们发现一种带螺纹的矿石,研究时发现该矿石(主要成分是FeS2)能在氧气中燃烧生成氧化铁和二氧化硫。该反应化学方程式为______。
(2)白色固体粉末氯酸钾(KClO3)在二氧化锰(MnO2)作催化剂并加热的条件下能生成氯化钾固体和氧气。该反应化学方程式为______。
(3)剧烈运动后血液中产生了较多乳酸(C3H6O3),使人肌肉酸痛,经过一段时间放松,由于乳酸与吸入的氧气反应,生成二氧化碳和水,酸痛感消失。该反应化学方程式为______。
【答案】4FeS2+11O2![]() 2Fe2O3+8SO2 2KClO3
2Fe2O3+8SO2 2KClO3![]() 2KCl+3O2↑ C3H6O3+ 3O2=3CO2+3H2O
2KCl+3O2↑ C3H6O3+ 3O2=3CO2+3H2O
【解析】
(1)FeS2能在氧气中燃烧生成氧化铁和二氧化硫,该反应化学方程式为:4FeS2+11O2![]() 2Fe2O3+8SO2;
2Fe2O3+8SO2;
(2)氯酸钾(KClO3)在二氧化锰(MnO2)作催化剂并加热的条件下能生成氯化钾固体和氧气,该反应化学方程式为:2KClO3![]() 2KCl+3O2↑;
2KCl+3O2↑;
(3)乳酸(C3H6O3)与吸入的氧气反应生成二氧化碳和水,该反应化学方程式为:C3H6O3+ 3O2=3CO2+3H2O。

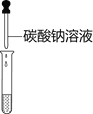
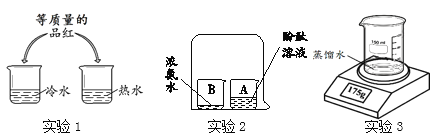
【题目】在一次化学兴趣小组活动中,老师拿来一瓶标签有破损的试剂瓶,如图,里面盛有一种无色溶液.该化学兴趣小组的同学对此展开探究:

(提出问题)这瓶无色溶液的溶质是什么呢?
(做出猜想)猜想一CaCO3;猜想二CaCl2;猜想三Ca(OH)2;猜想四Ca(NO3)2
(讨论交流)讨论后,大家一致认为猜想一是错误的,其理由是__________.
(查阅资料)CaCl2溶液、Ca(NO3)2溶液均是中性的.
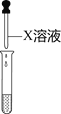
(实验探究)为验证其余猜想,小组的四位同学分别设计了如下实验:
实验编号 | 实验一 | 实验二 | 实验三 | 实验四 |
实验方案 |
|
|
|
|
实验现象 | 产生白色沉淀 | 产生白色沉淀 | ||
实验结论 | 猜想三成立 | 猜想三成立 | 猜想三成立 | 猜想三成立 |
(得出结论)猜想三成立,此无色溶液为Ca(OH)2溶液.
(表达交流)(1)实验一的现象是___________.
(2)实验二的化学反应方程式为_______________.
(3)小组同学经过讨论,一至认为实验三不能证明猜想三成立,其理由是_____________.
(拓展迁移)(4)实验四中的X溶液可以选择__________(填字母序号)溶液.
(5)你认为取用化学试剂时为防止标签受损,倾倒液体时应__________.
【题目】高锰酸钾在生产、生活中有广泛应用,实验小组对高锰酸钾的某些性质进行研究。 Ⅰ.不稳定性
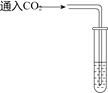
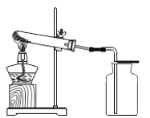
(1)如图所示进行实验,KMnO4受热分解的化学方程式为 ______,该装置的一处明显错误是______________;.
(2)可用如图方法收集O2时检验已经收集满氧气的方法______.
Ⅱ.腐蚀性
(查阅资料)KMnO4 溶液呈中性、有腐蚀性
(进行实验)实验 1:
KMnO4 溶液浓度 | 0.002% | 0.01% | 0.1% | 1% |
鸡皮的变化 | 无明显变化 | 边缘部分变为棕黄色 | 全部变为棕色 | 全部变为黑色 |
实验 2:将铜片分别浸泡在下列 4 种溶液中,现象如下表。
编号 | ① | ② | ③ | ④ | |
实验 |
25mL0.1% KMnO4 溶液 |
25mL0.1%KMnO4 溶 液+10 滴浓硫酸 |
25mL 蒸馏水 +10 滴浓硫酸 |
25mL1%KMnO4 溶 液+10 滴浓硫酸 | |
铜 片 质 量 /g | 实验前 | 0.54 | 0.54 | <>0.54 | 0.54 |
18 小时后 | 0.54 | 0.52 | 0.54 | 0.43 | |
(解释与结论)
(3)实验 1 的目的是______.
(4)实验 2 中通过对比②和④,得出的结论是__________.
(5)实验 2 中,欲得出“KMnO4 和硫酸共同作用对铜才有腐蚀性”的结论,需要对比______(填编号).
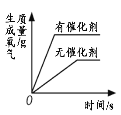
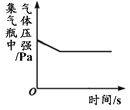
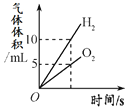
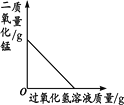
【题目】下列图像能正确反映对应变化关系的是
|
|
|
|
A.用等质量、等浓度的双氧水制取氧气 | B.利用红磷燃烧测定空气中氧气的含量(打开止水夹前) | C.将水通电电解一段时间 | D.向一定量的二氧化锰中加入过氧化氢溶液 |
A. A B. B C. C D. D