题目内容
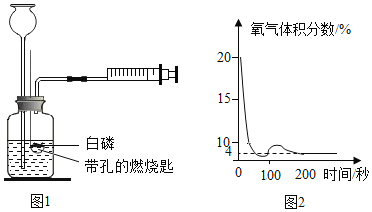
【题目】某同学进行了如下实验,验证一氧化碳与氧化铜的反应
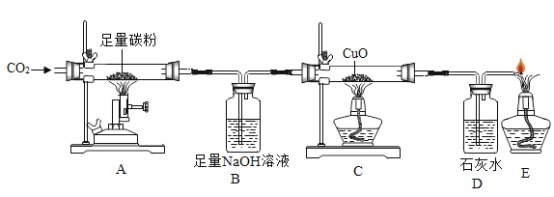
①进入装置 B 的气体中含有二氧化碳和_____
②C 处氧化铜发生反应的化学方程式是_____;D 中观察到的现象是______
③对于该实验的相关分析,正确的是_____(选填编号)
a 实验开始时,先缓慢通入二氧化碳,D 中无明显现象
b 装置 B 中无明显现象,说明该装置中没有发生反应
c 装置 E 的作用是将尾气点燃,防止污染空气
d 实验结束后,装置 C 玻璃管中固体减少的质量等于装置 D 中增加的质量
【答案】一氧化碳 ![]() 澄清石灰水变浑浊 ac
澄清石灰水变浑浊 ac
【解析】
①二氧化碳与碳在高温的条件下反应生成一氧化碳,故进入装置 B 的气体中含有二氧化碳和一氧化碳;
②C处氧化铜和一氧化碳在加热的条件下反应生成铜和二氧化碳,该反应的化学方程式为:![]() ;
;
C处产生的二氧化碳能与氢氧化钙反应生成碳酸钙和水,故D处观察到的现象是:澄清石灰水变浑浊;
③a、实验开始时,先缓慢通入二氧化碳,二氧化碳被B处的氢氧化钠吸收,C处无二氧化碳生成,故D处无明显现象,符合题意;
b、装置B中氢氧化钠与二氧化碳反应生成了碳酸钠和水,无明显现象,不符合题意;
c、一氧化碳有毒,排放到空气中会污染空气,故装置E的作用是处理尾气,防止污染空气,符合题意;
d、![]() ,
,![]() ,实验结束后,装置 C 玻璃管中固体减少的质量是氧化铜中氧元素的质量,装置 D 中增加的质量是装置C中反应生成的二氧化碳的质量,不相等,不符合题意。
,实验结束后,装置 C 玻璃管中固体减少的质量是氧化铜中氧元素的质量,装置 D 中增加的质量是装置C中反应生成的二氧化碳的质量,不相等,不符合题意。
故选ac。

【题目】真真实验小组欲亲自探究适合在实验室制取二氧化碳的药品。她们准备利用碳酸钠粉未、块状大理石、稀盐酸、浓盐酸、稀硫酸五种药品进行实验探究
(提出问题)上述药品间的相互反应都适合在实验室制取二氧化碳气体吗?
(方案设计)(1)经过讨论大家都致认为浓盐酸不适合用于实验室制取二氧化碳你认为原因是___。
(2)真真小组同学经过反复设计研究后确定迸行如下图所示的四个实验
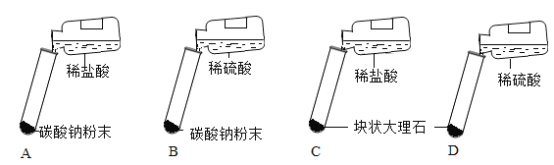
(结论分析)实验报告单如下表
实验编号 | 实验现象 | 实验结论 |
A | 剧烈反应,迅速产生大量气泡 | 反应速率过快,不便于气体收集 |
B | 剧烈反应,迅速产生大量气泡 | _________ |
C | ______ | 便于收集,适合在实验室制取CO2 |
D | 一开始产生气泡,之后便迅速减慢直到反应几乎停止 | 因为无法持续的产生气体,不适合用在实验室制取二氧化碳 |
(3)①结合上面的实验探究报告,可用于实验室制取二氧化碳气体的化学反应方程式为___;
②在确定实验室制取气体反应原理时,要考虑诸多因素,请你再写出一种需要考虑的因素:___;
(继续探究)在实验室里,小组同学利用12.3%的稀盐酸与块状大理石来制取二氧化碳。
(问题引入)(4)实验结束后发现裝置内废液中还有块状固体存在,但已观察不到气泡产生,反应后的废液中还有盐酸吗?甲同学用pH试纸测得该废液的pH=2,证明___;
(5)反应后废液中剩余的块状固体中还有碳酸钙吗?乙同学带着疑问取岀废液中块状的固体,洗净后放入试管中, 再加入约2mL的___, 立即产生大量的气泡, 证明___。
(猜想验证)(6)既然反应后废液中还有盐酸和碳酸钙,那为何观察不到实验现象呢?
①同学认为是废液中盐酸浓度太低,所以观察不到现象。甲同学将少许___置于试管中,加入约2mLpH=1的稀盐酸,立即观察到有气泡冒出
②乙同学认为是实验所用大理石块较大,与盐酸接触不充分,所以观察不到明显的现象,于是乙同学向老师要了一些纯净的碳酸钙粉未放入试管中,加入约2ml___,立即观察到有气泡冒出
(实验结论)
(7)依据(4)(5)确定发生反应后装置废液中的盐酸与碳酸钙共存,但不能观察到现象。结合实验(6)①②闸述其原因___;
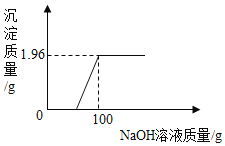
(拓展延伸)(8)实验室用块状大理石与稀盐酸反应 pH至气泡逸出不明显后,测得残留液 pH=2,若取适量残留液体的上层清液于试管中,逐滴滴入碳酸钠溶液至过量。请在下图中绘出变化趋势___。

【题目】下列对化学基本观念的归纳和分析不正确的是( )
A.变化观 | B.守恒观 |
①燃烧是化学变化,爆炸不一定是化学变化 ②有些化学变化没有明显的外在现象 | ①质量守恒的原因是化学反应中原子和分子的种类、质量不变 ②某物质燃烧生成二氧化碳和水,该物质一定含有碳、氢、氧元素 |
C.粒子观 | D.分类观 |
①金刚石、石墨是由原子构成的,C60 是由分子构成的 ②阴离子的质子数小于核外电子数 | ①冰水混合物和干冰都属于纯净物 ②反应 |
A.AB.BC.CD.D