题目内容
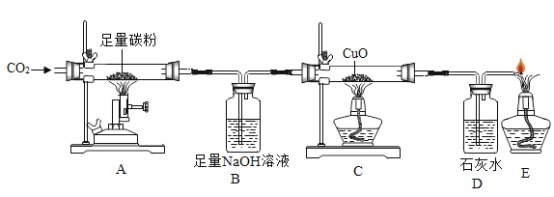
【题目】为测定空气里氧气的含量,甲、乙、丙三个同学用如图所示的装置分别进行了实验探究。
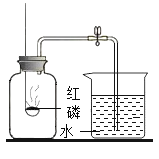
(1)甲同学:点燃红磷立即伸入瓶中并塞上瓶塞。待红磷燃烧停止并冷却后,打开止水夹,观察到集气瓶中吸入水测得体积约占集气瓶容积的__________________。
(2)乙同学:用碳替代红磷,完成上述实验,发现集气瓶内并没有吸入水,其原因是_________。
(3)丙同学:为完成乙同学的实验,丙同学向乙同学实验的集气瓶中加入少量的某溶液,得到了与甲同学相同的实验结果,丙同学所加试剂是________溶液。
【答案】![]() 碳燃烧生成物是二氧化碳气体,瓶内气压不变 NaOH
碳燃烧生成物是二氧化碳气体,瓶内气压不变 NaOH
【解析】
(1)红磷燃烧消耗装置内的氧气,导致瓶内压强变小,氧气约占空气体积的![]() ,待红磷燃烧停止并冷却后,打开止水夹,观察到集气瓶中吸入水的体积约占集气瓶容积的
,待红磷燃烧停止并冷却后,打开止水夹,观察到集气瓶中吸入水的体积约占集气瓶容积的![]() ;
;
(2)用碳替代红磷,完成上述试验,碳在空气中燃烧生成二氧化碳气体,瓶内气体体积变化不大,瓶内压强不变,故集气瓶内并没有吸入水;
(3)二氧化碳能被氢氧化钠溶液吸收,向集气瓶中加入少量的氢氧化钠溶液,二氧化碳与氢氧化钠溶液反应生成碳酸钠和水,而使瓶内压强变小,得到了与甲同学相同的实验结果。

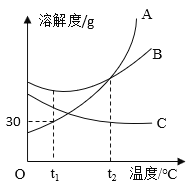
【题目】Ca(OH)2 和NaOH是重要的碱。在不同温度时的溶解度如下:
温度(°C) | 20 | 40 | 60 | 80 | |
溶解度(g/100g 水) | Ca(OH)2 | 0.17 | 0.14 | 0.09 | 0.08 |
NaOH | 109 | 129 | 174 | 314 | |
①20°C时Ca(OH)2的溶解度是_________。
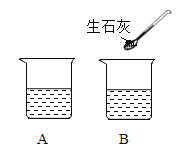
②A、B二只烧杯装有等质量的饱和石灰水(如图所示)。B烧杯中加入少量生石灰,写出发生反应的化学方程式___________。此时,A、B烧杯中溶液质量A__________B (选填“>”、“<”或“=”)。
③20°C时100g饱和NaOH溶液蒸发10g水后,恢复到原温度,析出___________gNaOH固体。
④60°C时NaOH饱和溶液中含少量Ca(OH)2,若要得到较纯净NaOH晶体,应采取的物理方法是________。
⑤若在20°C时,鉴别Ca(OH)2、NaOH饱和溶液,可选用的方法是_____________。
I 降低温度
II 滴加酚酞溶液
III 测pH
IV 滴入盐酸