题目内容
【题目】过氧化氢溶液常用于家庭、医疗等方面,它具有杀菌、漂白、防腐和除臭等作用。现有一瓶过氧化氢溶液,标签如图。

(1)实验室制取氧气时,要将30%的H2O2溶液稀释到6%,其可能原因是_____。
(2)家庭杀菌需配3%的过氧化氢溶液200g,则需30%的H2O2溶液体积_____mL(保留一位小数,下同),加水_____mL。
(3)涂到伤口处有白沫产生,这是因为伤口中有过氧化氢酶,请写出产生泡沫的化学方程式:_____。
【答案】浓度太大,反应速率太快,不利于反应的控制和气体的收集 18.2 180.0 2H2O2 2H2O+O2↑
2H2O+O2↑
【解析】
(1)反应物的浓度、纯度、温度等因素会影响反应速率,通常,浓度越大,反应越快,实验室制取氧气时,要将30%的H2O2溶液稀释到6%,其可能原因是浓度太大,反应速率太快,不利于反应的控制和气体的收集;
(2)溶液稀释前后溶质的质量不变,家庭杀菌需配3%的过氧化氢溶液200g,则需30%的H2O2溶液质量为:![]() =20g,体积为:
=20g,体积为:![]() ;加水的质量为200g-20g=180g, 体积为:
;加水的质量为200g-20g=180g, 体积为:![]() ;
;
(3)产生泡沫的化学反应是过氧化氢在过氧化氢酶的作用下分解生成水和氧气,方程式:2H2O2 2H2O+O2↑。
2H2O+O2↑。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】同学们用碳酸钠溶液和盐酸的反应验证质量守恒定律,实验后他们对残留废液的成分进行探究。
[推理假设]
上述两种物质发生反应的化学方程式为_______,由此推测出废液中一定有NaCl,可能有_______。
[实验探究]
(1)确定废液中是否含有盐酸:

①选择试剂:根据盐酸的化学性质,同学们选用了如图所示的五种物质,其中物质x是酸碱指示剂中的_____溶液。
②实验验证:某同学向废液中加入少量的铁粉,观察到_____, 确定废液中一定没有盐酸。
(2)确定废液中是否含有Na2CO3;某同学选用______测出废液的pH=10,确定废液中一定含有Na2CO3。
(3)处理废液,回收利用:欲从废液中得到纯净的NaCl,请完成如下实验方案设计。
方案 | 加入试剂 | 提纯的方法 | 方案评价 |
一 | 适量Ca(NO3)2溶液 | 过滤、 蒸发结晶 | ______(选填可行或不可行) |
二 | 稍过量的______ | ______ | 可行 |
(4)拓展运用:
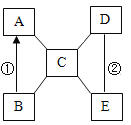
按如下图方案分离BaCl2和NaCl的固体混合物时,x溶液中溶质是_______。