题目内容
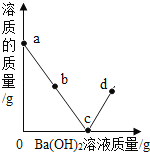
【题目】室温时,随着向盛有稀硫酸的烧杯中逐滴加入Ba(OH)2溶液,烧杯内溶液中的溶质质量变化如图所示(忽略溶液温度的变化),下列分析正确的是( )
A. a点溶液中有两种溶质
B. b点溶液中滴加紫色石蕊溶液,溶液变蓝
C. c点烧杯内液体的pH=7
D. d点溶液中较多的Ba2+、OH﹣、SO42﹣、H+
【答案】C
【解析】试题分析:向盛有稀硫酸的烧杯中逐滴加入Ba(OH)2溶液,会发生反应:H2SO4+Ba(OH)2=BaSO4↓+2H2O,当二者恰好完全反应时,得到的是沉淀和水。A.a点溶液中只有溶质H2SO4,错误;B.b点溶液中含有过量的硫酸,所以溶液显酸性,滴加紫色石蕊溶液,溶液变红色,错误;C.c点烧杯内二者恰好反应,溶液为中性,所以液体的pH=7,正确;D.d点溶液中含有溶质Ba(OH)2,溶液显碱性,所以其中有较多的Ba2+、OH-、,但是无大量的SO42-、H+,错误。

练习册系列答案
相关题目