题目内容
金属是现代生活、工业生产以及科学研究中应用极为普遍的一类材料.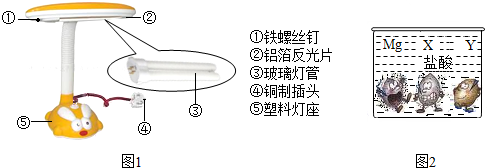
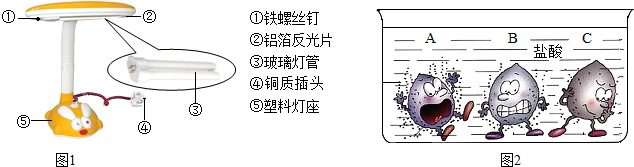
(1)青少年看书、写字一定要爱护眼睛,台灯是在光线不足时常用的照明用具.
①图1中标示的物质属于金属材料的有
②灯管后面的反光片为铝箔.铝块能制成铝箔是利用了铝的
③铝比铁活泼,但铝箔却比铁螺丝钉耐腐蚀,其原因是
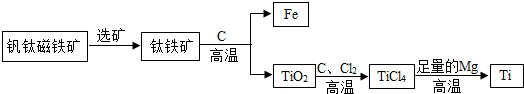
(2)已知在相同的条件下,金属的活动性越强,金属和酸反应产生气泡(氢气)的速度就越快.Mg、Cu、Fe三种金属在稀盐酸里的反应现象如右图2所示.
①右图中Y所代表的金属是
②Mg、Cu、Fe三种金属的活动性由强到弱的顺序为
(3)金属的开发和利用是人类文明和社会进步的标志.
①我国古代将炉甘石(ZnCO3)、赤铜矿(Cu2O)和木炭粉混合加热至800℃左右,即可得到与黄金外观相似的“药金”.
I.该方法不能制得金(Au)是因为
II.“药金”是
②钛因常温下不与酸、碱反应等优良的性能,被誉为“未来金属”.由钒钛磁铁矿提取金属钛的主要工艺过程如下:
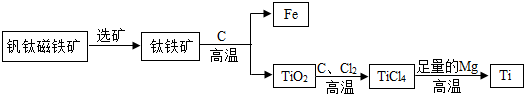
I.TiCl4在高温下与足量Mg反应置换生成金属Ti,该反应的化学方程式为:
II.上述生产过程中得到的金属钛中混有少量金属杂质,可加入
分析:(1)①根据金属材料包括金属单质及合金,从中找出金属材料;②利用金属的延展性可把金属压成片、拉成丝;③根据金属铝的化学性质,分析金属铝耐腐蚀的原因;
(2)由图示和金属活动性顺序可得;
(3)利用质量守恒定律中元素种类不变可以确定是否能得到金;依据转化过程可对钛的冶炼过程进行讨论.
(2)由图示和金属活动性顺序可得;
(3)利用质量守恒定律中元素种类不变可以确定是否能得到金;依据转化过程可对钛的冶炼过程进行讨论.
解答:解:(1)①金属单质及合金都属于金属材料,①铁螺丝钉、②铝箔反光片、④铜质插头都属于金属材料;
②利用金属铝具有良好的延展性可把金属铝制成片;
③铝在常温下能与空气中氧气反应,在其表现形成一层致密的氧化铝层,隔绝金属铝与氧气的进一步接触;
故答案为:(1)①:①②④;②延展;③铝与氧气反应表面形成致密氧化膜(表述合理即可);
(2)由图中Y表面没有气泡可得Y为金属铜;由实验现象可知三种金属的活动性由强到弱的顺序为Al、Fe、Cu
故填:①Cu,②:Mg>Fe>Cu
(3))①由质量守恒定律可知原反应物中无金元素,所以生成物种中不会有金元素,这种方法不能真正得到黄金;得到的药金应为锌-铜合金.
②在高温下TiCl4与足量Mg反应置换生成金属Ti,该反应的化学方程式为:TiCl4+2Mg
Ti+2MgCl2.
上述生产过程中得到的金属钛中混有的少量金属杂质为铁和镁,所以可加入稀盐酸或稀硫酸除去.
故答案为:①Ⅰ:反应物中不含有金元素;Ⅱ:合金;
②I:TiCl4+2Mg
Ti+2MgCl2; II:稀盐酸(或稀硫酸).
②利用金属铝具有良好的延展性可把金属铝制成片;
③铝在常温下能与空气中氧气反应,在其表现形成一层致密的氧化铝层,隔绝金属铝与氧气的进一步接触;
故答案为:(1)①:①②④;②延展;③铝与氧气反应表面形成致密氧化膜(表述合理即可);
(2)由图中Y表面没有气泡可得Y为金属铜;由实验现象可知三种金属的活动性由强到弱的顺序为Al、Fe、Cu
故填:①Cu,②:Mg>Fe>Cu
(3))①由质量守恒定律可知原反应物中无金元素,所以生成物种中不会有金元素,这种方法不能真正得到黄金;得到的药金应为锌-铜合金.
②在高温下TiCl4与足量Mg反应置换生成金属Ti,该反应的化学方程式为:TiCl4+2Mg
| ||
上述生产过程中得到的金属钛中混有的少量金属杂质为铁和镁,所以可加入稀盐酸或稀硫酸除去.
故答案为:①Ⅰ:反应物中不含有金元素;Ⅱ:合金;
②I:TiCl4+2Mg
| ||
点评:本题除了考查金属以及金属材料的性质和活动性顺序,还多方面开放性的考查灵活运用知识的能力.

练习册系列答案
相关题目
 金属是现代生活和工业生产中应用极为普遍的一类材料.
金属是现代生活和工业生产中应用极为普遍的一类材料.(1)已知在相同的条件下,金属的活动性越强,金属和酸反应产生气泡(氢气)的速度就越快.Al、Cu、Fe三种金属在稀盐酸里的反应现象如右图所示.
①右图中Y所代表的金属是
②Al、Cu、Fe三种金属的活动性由强到弱的顺序为
③铝是一种活泼金属,但常温下铝却有较强的抗腐蚀性,其原因是
(2)金属的开发和利用是人类文明和社会进步的标志.
①我国古代将炉甘石(ZnCO3)、赤铜矿(Cu2O)和木炭粉混合加热至800℃左右,即可得到与黄金外观相似的“药金”.
I.用上述方法不能制得真正的黄金(Au)是因为
II.“药金”是
②钛因常温下不与酸、碱反应等优良的性能,被誉为“未来金属”.由钒钛磁铁矿提取金属钛的主要工艺过程如下:

在高温下与足量Mg反应置换生成金属Ti,该反应的化学方程式为:
上述生产过程中得到的金属钛中混有少量金属杂质,可加入
(3)已知某金属粉末中除含有Al外还含有一定量的Fe和Cu,为证明Fe和Cu的存在并测定其中Al的质量分数,某化学兴趣小组的同学展开了如下的实验探究.
资料在线:Al与氢氧化钠溶液反应生成溶于水的偏铝酸钠和氢气(反应的化学方程式为:2Al+2H2O+2NaOH=2NaAlO2+3H2↑),Fe和Cu不与氢氧化钠溶液反应.
①请完成证明金属粉末中存在Fe和Cu的实验设计:
| 实验操作 | 实验现象 | 结论 |
| Ⅰ取少量的金属粉末于试管中,加入足量的 |
仅除去铝 | |
| Ⅱ将试管静置,弃去上层清液,加入足量的稀硫酸. | 证明含有铁 | |
| Ⅲ将试管静置,弃去上层清液,多次洗涤剩余固体 | 剩余固体呈紫红色 | 证明含有铜 |
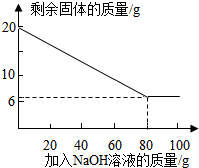 ②为探究该金属粉末中Al的质量分数,取20 g该金属粉末,把100 g氢氧化钠溶液平均分成5份依次加入,充分反应后,过滤出固体,将其洗涤、干燥、称量.实验过程中得到的部分数据与图象如下:
②为探究该金属粉末中Al的质量分数,取20 g该金属粉末,把100 g氢氧化钠溶液平均分成5份依次加入,充分反应后,过滤出固体,将其洗涤、干燥、称量.实验过程中得到的部分数据与图象如下:| 加NaOH溶液的次数 | 第一次 | 第二次 | 第三次 | … |
| 剩余固体的质量/g | 16.5 | n | 9.5 | … |
Ⅱ.该金属粉末中Al的质量分数为
Ⅲ.列式计算:所用氢氧化钠溶液的溶质质量分数为多少?
金属是现代生活和工业生产中应用极为普遍的一类材料.
已知某金属粉末中除含有Al外还含有一定量的Fe和Cu,为证明Fe和Cu的存在并测定其中Al的质量分数,某化学兴趣小组的同学展开了如下的实验探究.
(查阅资料)Al与氢氧化钠溶液反应生成溶于水的偏铝酸钠和氢气(反应的化学方程式为:2Al+2H2O+2NaOH=2NaAlO2+3H2↑),Fe和Cu不与氢氧化钠溶液反应.
①请完成证明金属粉末中存在Fe和Cu的实验设计:
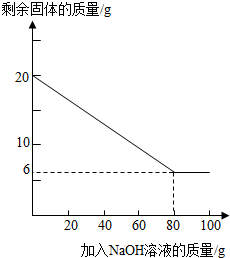
②为探究该金属粉末中Al的质量分数,取20g该金属粉末,把100g氢氧化钠溶液平均分成5份依次加入,充分反应后,过滤出固体,将其洗涤、干燥、称量.实验过程中得到的部分数据与图象如下:
I.分析以上数据可知上表中n的值为 ;
II.该金属粉末中Al的质量分数为 %;
III.列式计算:所用氢氧化钠溶液的溶质质量分数为多少?
已知某金属粉末中除含有Al外还含有一定量的Fe和Cu,为证明Fe和Cu的存在并测定其中Al的质量分数,某化学兴趣小组的同学展开了如下的实验探究.
(查阅资料)Al与氢氧化钠溶液反应生成溶于水的偏铝酸钠和氢气(反应的化学方程式为:2Al+2H2O+2NaOH=2NaAlO2+3H2↑),Fe和Cu不与氢氧化钠溶液反应.
①请完成证明金属粉末中存在Fe和Cu的实验设计:
| 实验操作 | 实验现象 | 结论 |
| Ⅰ取少量的金属粉末于试管中,加入足量的________________(填试剂名称). | _____________. | 仅除去铝 |
| Ⅱ将试管静置,弃去上层清液,加入足量的稀硫酸. | _____________. | 证明含有铁 |
| Ⅲ将试管静置,弃去上层清液,多次洗涤剩余固体 | 剩余固体呈紫红色 | 证明含有铜 |
| 加NaOH溶液的次数 | 第一次 | 第二次 | 第三次 | … |
| 剩余固体的质量/g | 16.5 | n | 9.5 | … |
II.该金属粉末中Al的质量分数为
III.列式计算:所用氢氧化钠溶液的溶质质量分数为多少?