题目内容
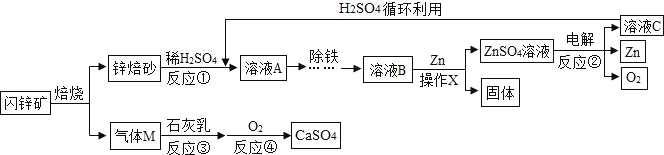
【题目】氯化亚铜(CuCl)是一种难溶于水和乙醇,在潮湿空气中易变质,广泛应用于冶金、电镀、医药等行业的原料。CuCl的制备流程如下:
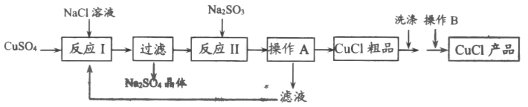
(1)“反应Ⅰ”中发生的化学方程式为_______。
(2)反应Ⅰ“过滤”后所得的滤液中,除了Cu2+, Na+, Cl-外,还存在较多的离子是_______(写离子符号)
(3)“反应Ⅱ”中发生的化学变化是2CuCl2+Na2SO3 +H2O =2CuCl↓+2NaCl+ H2SO4,其中化合价发生改变的元素有_______;反应过程中溶液的pH_______(选填“变大”、“变小”或“不变”)。
(4)本流程中可以循环利用的物质是_______。(写名称)
(5)在洗涤过程中用乙醇而不用水洗涤的原因是_______。
(6)“操作B”的名称是_______。
【答案】CuSO4+2NaCl=CuCl2+Na2SO4↓ SO42- Cu、S 减小 氯化钠 保证CuCl表面干燥,防止潮湿空气中变质 干燥
【解析】
(1)硫酸铜和氯化钠反应生成硫酸钠和氯化铜,化学方程式为:CuSO4+2NaCl=CuCl2+Na2SO4↓;
(2)“滤液1”中主要物质是硫酸钠和氯化铜,所以“过滤”后所得的滤液中,除了Cu2+、Na+、Cl-外,还存在较多的离子是SO42-;
(3)在反应Ⅱ中,铜元素的化合价从+2变成了+1,硫元素的化合价从+4变成了+6,反应前后,钠元素的化合价是+1,氧元素的化合价是-2,钠元素的化合价是+1,氢元素的化合价是+1,所以化合价发生改变的元素有:Cu、S,反应过程中生成了硫酸,溶液的pH减小;
(4)本流程中可以循环利用的物质(水除外)是氯化钠;
(5)氯化亚铜(CuCl)是一种难溶于水和乙醇,在潮湿空气中易变质,所以在洗涤过程中用乙醇而不用水洗涤的原因是:保证CuCl表面干燥,防止潮湿空气中变质;
(6)氯化亚铜洗涤后,经过干燥可以得到氯化亚铜晶体,所以操作B是干燥。

【题目】将一定量的丙醇(C3H8O)和氧气置于一个封闭的容器中引燃,其反应的化学方程式为: aC3H8O+bO2![]() cCO2+dH2O+eX,测得反应前后各物质的质量如下表:
cCO2+dH2O+eX,测得反应前后各物质的质量如下表:
物质 | 丙醇 | 氧气 | 水 | 二氧化碳 | X |
反应前质量/g | 6.0 | 12.8 | 0 | 0 | 0 |
反应后质量/g | 0 | 0 | 7.2 | 8.8 | x |
下列判断正确的是( )
A. 表中x的值为1.8B. x可能是该反应的催化剂
C. X可能为甲烷D. 方程式中a:b=1:4
【题目】20℃时,NaCl溶解情况见下表,相关叙述正确的是
实验 序号 | 水的 质量(g) | 加入NaCl 的质量(g) | 溶液的 质量(g) |
① | 10.0 | 1.5 | 11.5 |
② | 10.0 | 3.0 | 13.0 |
③ | 10.0 | 4.5 | 13.6 |
④ | 10.0 | 6.0 | 13.6 |
A. ①所得溶液的溶质质量分数为15.0%
B. ②中所得溶液是饱和溶液
C. 20℃时,NaCl 的溶解度是45.0g/100g 水
D. ③④溶液的溶质质量分数相等