��Ŀ����
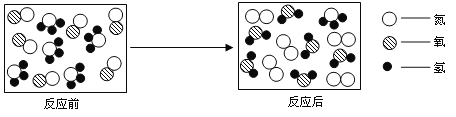
����Ŀ����һ�����ı�����C3H8O������������һ����յ���������ȼ���䷴Ӧ�Ļ�ѧ����ʽΪ: aC3H8O+bO2![]() cCO2+dH2O+eX����÷�Ӧǰ������ʵ��������±���
cCO2+dH2O+eX����÷�Ӧǰ������ʵ��������±���
���� | ���� | ���� | ˮ | ������̼ | X |
��Ӧǰ����/g | 6.0 | 12.8 | 0 | 0 | 0 |
��Ӧ������/g | 0 | 0 | 7.2 | 8.8 | x |
�����ж���ȷ���ǣ� ��
A. ����x��ֵΪ1.8B. x�����Ǹ÷�Ӧ�Ĵ���
C. X����Ϊ����D. ����ʽ��a:b=1:4
���𰸡�D
��������
A��x=6.0+12.8-7.2-8.8=2.8����ѡ��˵������ȷ��
B��X��Ӧ���������ӣ����������ѡ��˵������ȷ��
C��X����Ԫ������Ϊ��6.0g��![]() -7.2g��
-7.2g��![]() =0�������к�����Ԫ�أ����X���Ǽ��飬��ѡ��˵������ȷ��
=0�������к�����Ԫ�أ����X���Ǽ��飬��ѡ��˵������ȷ��
D����Ӧ�����У������������Ļ�ѧ������֮��Ϊ��![]() ��
��![]() =1��4����ѡ��˵����ȷ��
=1��4����ѡ��˵����ȷ��
��ѡD��

��ϰ��ϵ�д�
�����Ŀ