题目内容
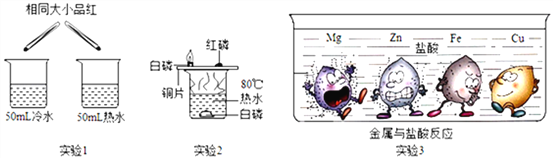
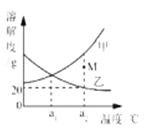
【题目】结合图片判断下列说法不正确的是( )

A. 图中镁与盐酸的反应速率最快
B. 图中能体现出四种金属的活动性由弱到强的顺序是Mg、Zn、Fe、Cu
C. 此实验应该保证金属与盐酸的接触面积相同
D. 金属活动性的强弱可以依据金属是否与酸反应及反应的剧烈程度来确定
【答案】B
【解析】A、由图可以看出,镁冒气泡最剧烈,镁与盐酸的反应速率最快,故A正确;B、由图可以看出,镁冒气泡最剧烈,其次是锌和铁,铜不冒气泡,活动性最弱,图中能体现出四种金属的活动性由弱到强的顺序是Cu、Fe、Zn、Mg,故B不正确;C、此实验应该保证金属与盐酸的接触面积相同,才能比较金属的活动性强弱,故C正确D、金属活动性的强弱可以依据金属是否与酸反应及反应的剧烈程度来确定,故D正确。故选B。

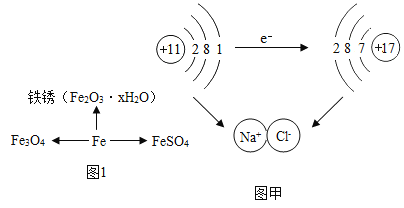
【题目】小明在做铁与硫酸溶液反应的实验时,发现生成的气体有刺激性气味,于是进行了探究。
【提出问题】铁与硫酸溶液反应生成的气体为什么有刺激性气味?
【查阅资料】 (1)6H2SO4(浓)+ 2Fe![]() Fe2(SO4)3 + 6H2O + 3SO2↑
Fe2(SO4)3 + 6H2O + 3SO2↑
(2)SO2可使品红溶液的红色褪去
【进行猜想】铁与不同浓度的硫酸溶液反应,生成的气体可能有二氧化硫
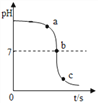
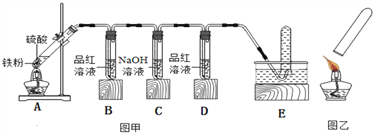
【实验探究】小明用图甲所示装置进行实验,并将E中收集到的气体进行如图乙所示的爆鸣实验。请帮助小明完成下表:
A中硫 酸浓度 | 实验现象 | A中生成气体成分 | |||
B中品红溶液 | D中品红溶液 | 爆鸣实验 | |||
实验一 | 98% | ___________ | 不褪色 | 无爆鸣声 | 只有SO2 |
实验二 | 45% | 稍有褪色 | 不褪色 | 有爆鸣声 | __________ |
实验三 | 25% | ___________ | 不褪色 | ________ | 只有H2 |
【实验结论】_____________________________________________________。
【交流反思】
实验一中C装置的作用是_______,写出C装置中发生反应的化学方程式__________。
【拓展延伸】已知:CO2和SO2既有相似性也有差异性。
气体 | CO2 | SO2 | |
相似性 | 与澄清石灰水反应 | 二者都产生白色浑浊 | |
差异性 | 与KMnO4溶液 | 不反应 | 气体被吸收,溶液逐渐褪色 |
化石燃料的气体产物中有CO2和SO2等物质。结合已知信息,请你设计实验证明化石燃料燃烧的气体产物中有CO2(写出操作、试剂、现象、结论)__________________。