题目内容
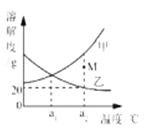
【题目】右图是甲、乙两种固体物质(不含结晶水)的溶解度曲线。下列说法正确的是
A.甲的溶解度大于乙的溶解度
B.a1℃时,甲、乙饱和溶液的温度升温至a2℃时,均有固体析出
C.a2℃时,M点对应的甲溶液不饱和
D.a2℃时,乙饱和溶液的质量分数为20%
【答案】C
【解析】A、比较溶解度的大小要指明温度,错误;B、甲的溶解度随温度的升高而增大,乙的溶解度随温度的升高而减小,故a1℃时,甲、乙饱和溶液的温度升温至a2℃时,乙中有固体析出,甲中没有,错误;C、溶解度曲线上的点对于的是该温度下的饱和溶液,曲线下方的点表示的是该温度下的不饱和溶液,故a2℃时,M点对应的甲溶液不饱和,正确;D、a2℃时,乙的溶解度为20g,那么它的饱和溶液的溶质质量分数=![]() 16.7%,错误。故选C。
16.7%,错误。故选C。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目