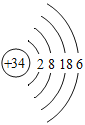
��Ŀ����
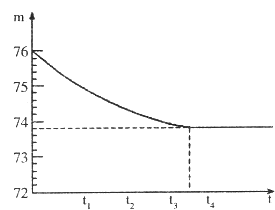
����Ŀ��ij��ѧ��ȤС����ʵ�������������ʵ�飺
��������ȡ������������30%���ܶ�Ϊ1.15g/mL�Ľ�Ũ����40mL��60mL����ˮ�������ϡ���ᣬ��ʯ��ʯ��Ӧ�Ƶ����壬��������ͨ�����ʯ��ˮ��һֱδ�����dz��֡�Ϊ�ˣ����������ʦ����ʦ��������ΪŪ��ԭ�����ʵ��̽��������������̽���Ĺ��̣�����������������
��������⣩Ϊʲô�Ƶõ����岻��ʹʯ��ˮ����ǣ�
��ʵ��̽����
��������� | ʵ�鲽�� | ʵ������ | ʵ����� |
������ ʯ�� ˮ�Ѿ���ȫ���� | ��ȡ����ʵ������ʯ��ˮ���Թ��У��μ�________�Լ� | ��Һ���ɫ | ˵��������________ |
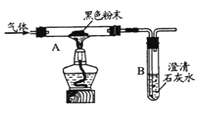
������ �������л���HCl | ���Ƶõ�����ֱ��ͨ��װ������________�����Һ���Թ��� | ________ | ˵�������� ��ȷ |
���������ۣ�
��1����С��ͬѧ���ۺ���Ϊ����������ͨ�����ʯ��ˮ��һֱδ������������֡�ԭ����________��
��2����������Ũ�ȴ�________%��Ӧ����������ϡ�͡�
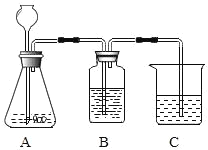
��3��������ͼװ����ɲ�����������ʵ��̽������B�������Լ���������________��C�е�����________��
���𰸡���ɫ��̪ ���� ϡ������������ ������ɫ���� ����ӷ��������Ȼ�����������ˮ�γ����ᣬ�������������Ʒ�Ӧ������û�й۲쵽����� 13 �����Ȼ��Ⲣ�����Ȼ��� �����ʯ��ˮ�����
��������
�⣺��ʵ��̽����ʯ��ˮ�е�������������ȫ���ʣ�������������������еĶ�����̼��Ӧ����̼��Ƴ�����ˮ����ʱҺ������ԣ�����ʹ��ɫ��̪��Һ���ɫ������ʵ������ȡ����ʵ������ʯ��ˮ���Թ��У��μ���ɫ��̪��Һ����Һ����˺�ɫ��˵��ʯ��ˮδ��ȫ���ʣ�������������
������лӷ��ԣ��ӷ��������Ȼ�����������ˮ�γ����ᣬ����������������Һ��Ӧ���ɲ�����ϡ������Ȼ�����ɫ����������������ȷ����ʵ�����Ϊ�����Ƶõ�����ֱ��ͨ��װ������ϡ�����������������Һ���Թ��У���۲쵽�а�ɫ�������������
��������� | ʵ�鲽�� | ʵ������ | ʵ����� |
������ʯ�� ˮ�Ѿ���ȫ���� | ��ȡ����ʵ������ʯ��ˮ���Թ��У��μ� ��ɫ��̪�Լ� | ��Һ���ɫ | ˵�������� ���� |
�������������л���HCl | ���Ƶõ�����ֱ��ͨ��װ������ϡ�����������������Һ���Թ��� | ������ɫ���� | ˵����������ȷ |
���������ۡ�
��1��������лӷ��ԣ����ӷ����Ȼ������壬�Ȼ�����������ˮ�����ᣬʯ��ˮδ����ǵ�ԭ����![]() ������HClʱCO2�����Ca��OH��2��Ӧ�����ʯ��ˮδ����ǡ��������ӷ��������Ȼ�����������ˮ�γ����ᣬ�������������Ʒ�Ӧ������û�й۲쵽����ǣ�
������HClʱCO2�����Ca��OH��2��Ӧ�����ʯ��ˮδ����ǡ��������ӷ��������Ȼ�����������ˮ�γ����ᣬ�������������Ʒ�Ӧ������û�й۲쵽����ǣ�
��2��������������30%���ܶ�Ϊ1.15g/mL�Ľ�Ũ����40mL��60mL����ˮ�������ϡ���ᣬ���Ƶ�ϡ���������ʵ���������Ϊ��![]() ��100%��13%�����13��
��100%��13%�����13��
��3������Cl������AgNO3��Һ�������Ȼ�����ڣ�AgNO3��Һ����ǣ����Bƿ������������Һ���Լ����Ȼ��Ⲣ�����Ȼ��⣬��Bƿ�ڵ���Һ�в�����ɫ������˵�������� ��ȷ��Cʢ��ʵ�����õij���ʯ��ˮ���������ʯ��ˮ����ǣ�˵�������� ����������Ȼ��Ⲣ�����Ȼ��⣻�����ʯ��ˮ����ǡ�