题目内容
【题目】某汽车安全气囊的产气药剂主要含有Fe2O3、KClO4、NaHCO3、NaN3等物质,当汽车发生碰撞时,产气药剂产生大量的气体使气囊迅速膨胀,从而起到保护作用。
(1)NaN3是气体发生剂,受热分解产生Na和一种气体,该气体是_____
(2)Fe2O3是主氧化剂,与Na反应生成Fe和Na2O,该反应属于_____反应。
(3)KClO4是助氧化剂,与Na反应生成KCl、Na2O,该反应中氯元素化合价_____。(填“不变”或“升高”或“降低”)
(4)NaHCO3是冷却剂,吸收产气过程中释放的热量而发生分解,其化学方程式为_____。
【答案】N2 置换 降低 ![]()
【解析】
(1)根据化学反应前后元素种类不变,故NaN3受热分解产生Na和氮气,氮气的化学式是:N2;
(2)Fe2O3与Na反应生成Fe和Na2O,符合置换反应的特点,故属于置换反应;
(3)KClO4中钾为+1价,氧为﹣2价,由化合价代数和为0的原则,氯为+7价,在KCl中,氯为﹣1价,因此该反应中氯元素化合价降低;
(4)碳酸氢钠受热分解生成碳酸钠和水和二氧化碳,化学方程式是:![]() 。
。

【题目】某化学兴趣小组在实验室里进行以下实验:
他们首先取溶质质量分数30%、密度为1.15g/mL的较浓盐酸40mL与60mL蒸馏水混合配制稀盐酸,跟石灰石反应制得气体,将此气体通入澄清石灰水,一直未见浑浊出现。为此,他们请教老师,老师建议他们为弄明原因进行实验探究。下面是他们探究的过程,请你帮助填答补充完整。
(提出问题)为什么制得的气体不能使石灰水变浑浊?
(实验探究)
猜想与假设 | 实验步骤 | 实验现象 | 实验结论 |
猜想① 石灰 水已经完全变质 | 吸取少量实验所用石灰水于试管中,滴加________试剂 | 溶液变红色 | 说明猜想①________ |
猜想② 该气体中混有HCl | 将制得的气体直接通入装有少量________混合溶液的试管中 | ________ | 说明猜想② 正确 |
(分析结论)
(1)该小组同学讨论后认为,将此气体通入澄清石灰水,一直未见浑浊现象出现。原因是________。
(2)所配盐酸浓度达________%,应当将其再行稀释。
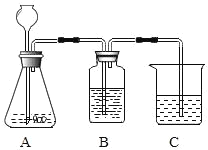
(3)若用如图装置完成猜想①、②的实验探究,则B中所加试剂的作用是________,C中的现象________。