题目内容
【题目】用化学符号或化学方程式表示:
(1)氨气________;
(2)烧碱_________;
(3)4个氢分子________;
(4)澄清石灰水中溶质的化学式________;
(5)氯化铁中的阳离子________;
(6)碳酸钠和氢氧化钙反应_______;
(7)一氧化碳还原氧化铁________;
(8)硫酸铜和氢氧化钠反应________。
【答案】NH3 NaOH 4H2 Ca(OH)2 Fe3+ ;Ca(OH)2+Na2CO3═CaCO3↓+2NaOH Fe2O3+3CO![]() 2Fe+3CO2 2NaOH+CuSO4═Cu(OH)2↓+Na2SO4
2Fe+3CO2 2NaOH+CuSO4═Cu(OH)2↓+Na2SO4
【解析】
(1)氨气的化学式为NH3,故填:NH3;
(2)烧碱是氢氧化钠,故填:NaOH;
(3)4个氢分子就是在氢气化学式的前面加上数字4,故填:4H2;
(4)澄清石灰水中溶质是氢氧化钙,故填:Ca(OH)2;
(5)氯化铁中的阳离子是铁离子,故填:Fe3+;
(6)碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,故填;Ca(OH)2+Na2CO3═CaCO3↓+2NaOH;
(7)一氧化碳还原氧化铁生成铁和二氧化碳,故填:Fe2O3+3CO![]() 2Fe+3CO2;
2Fe+3CO2;
(8)硫酸铜和氢氧化钠反应生成氢氧化铜沉淀和硫酸钠,故填:2NaOH+CuSO4═Cu(OH)2↓+Na2SO4。

【题目】某化学兴趣小组在实验室里进行以下实验:
他们首先取溶质质量分数30%、密度为1.15g/mL的较浓盐酸40mL与60mL蒸馏水混合配制稀盐酸,跟石灰石反应制得气体,将此气体通入澄清石灰水,一直未见浑浊出现。为此,他们请教老师,老师建议他们为弄明原因进行实验探究。下面是他们探究的过程,请你帮助填答补充完整。
(提出问题)为什么制得的气体不能使石灰水变浑浊?
(实验探究)
猜想与假设 | 实验步骤 | 实验现象 | 实验结论 |
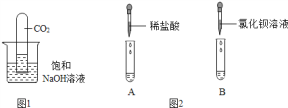
猜想① 石灰 水已经完全变质 | 吸取少量实验所用石灰水于试管中,滴加________试剂 | 溶液变红色 | 说明猜想①________ |
猜想② 该气体中混有HCl | 将制得的气体直接通入装有少量________混合溶液的试管中 | ________ | 说明猜想② 正确 |
(分析结论)
(1)该小组同学讨论后认为,将此气体通入澄清石灰水,一直未见浑浊现象出现。原因是________。
(2)所配盐酸浓度达________%,应当将其再行稀释。
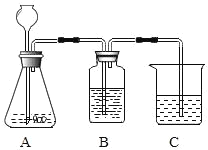
(3)若用如图装置完成猜想①、②的实验探究,则B中所加试剂的作用是________,C中的现象________。