题目内容
某同学做了如下图所示的实验,在14.6%的稀盐酸中加入碳酸钙,后加入10.6%的碳酸钠溶液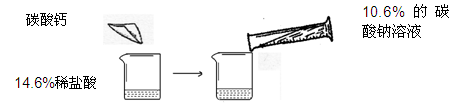
| | 第一次 | 第二次 |
| 14.6%的稀盐酸的质量 | m | m |
| 加入碳酸钙的质量 | 10g | 20g |
| 加入10.6%的碳酸钠溶液的质量 | 100g | 200g |
| 加入碳酸钠溶液后,实验现象 | 只有气泡 | 只有白色沉淀 |
写出实验一中发生化学反应的方程式
第一次实验中加入碳酸钙后溶液中溶质成分
根据已知条件列出求解第二次实验生成沉淀的质量的比例式
实验中加入稀盐酸m的质量为
若将第二次反应后的溶液蒸发191.2g水,则所得不饱和溶液中溶质的质量分数为
若用溶质质量分数29.2%的浓盐酸配置实验所需的稀盐酸,则需要加水的质量
(1)CaCO3+2HCl==CaCl2+H2O+CO2↑和Na2CO3+2HCl==2NaCl+H2O+CO2↑
(2)氯化钙、氯化氢 (3)106:100=21.2g:X
(4)100g (5)23.4% (6)100g
解析试题分析:(1)实验一在加入碳酸钠溶液后,只有气泡产生,说明盐酸过量,所以发生反应的化学方程式:CaCO3+2HCl==CaCl2+H2O+CO2↑和Na2CO3+2HCl==2NaCl+H2O+CO2↑
(2)根据上面的分析,盐酸过量,加上生成的氯化钙,所以第一次实验中加入碳酸钙后溶液中溶质成分:氯化钙、氯化氢
(3)根据实验一的数据,可以判断20g的碳酸钙与稀盐酸恰好完全反应,故生成的白色沉淀全部是氯化钙与加入的碳酸钠溶液反应生成的碳酸钙,方程式为:CaCl2+Na2CO3==CaCO3↓+2NaCl,根据Na2CO3与CaCO3的质量关系为106:100,而碳酸钠的质量=200g×10.6%=21.2g,所以第二次实验生成沉淀的质量的比例式:106:100=21.2g:X
(4)根据分析,加入20g的碳酸钙恰好能与稀盐酸反应,所以根据方程式:CaCO3+2HCl==CaCl2+H2O+CO2↑中CaCO3与HCl的质量关系为100:73,
解:CaCO3+2HCl==CaCl2+H2O+CO2↑
100 73
20g 14.6%×m
100:73=20g:14.6%×m
m=100g
(5)根据第(3)问分析,20g的碳酸钙与稀盐酸恰好完全反应:CaCO3+2HCl==CaCl2+H2O+CO2↑,根据CaCO3与CO2的质量关系100:44,可计算出产生二氧化碳的质量为8.8g,而生成的白色沉淀全部是氯化钙与加入的碳酸钠溶液反应生成的碳酸钙,方程式为:CaCl2+Na2CO3==CaCO3↓+2NaCl,根据Na2CO3与CaCO3、NaCl的质量关系,分别计算出CaCO3、NaCl的质量
解:设CaCO3、NaCl的质量分别为x、y
CaCl2+Na2CO3==CaCO3↓+2NaCl
106 100 117
200g×10.6% x y
106 : 100="200g×10.6%" :x
x=20g
106 : 117="200g×10.6%" :y
y=23.4g
所以反应后溶液质量=100g+20g-8.8g+200g-20g=291.2g
故将第二次反应后的溶液蒸发191.2g水,则所得不饱和溶液中溶质的质量分数=23.4g/291.2g-191.2g×100%=23.4%
(6)因为两次实验总共消耗盐酸溶液质量为200g,根据溶液稀释过程中,溶质的质量不变,可设需要浓盐酸的质量为a,可列式为:a×29.2%=200×14.6%,所以a=100g,所以需要加水的质量=200g-100g=100g
考点:酸碱盐的性质,根据化学方程式计算

小明在实验室发现一瓶氢氧化钠固体没有塞上瓶塞,于是他和他的同学一起对这瓶氢氧化钠固体展开探究,请你与他们一起进行探究。
【提出问题】这瓶氢氧化钠固体是否变质?
【查阅资料】CaCl2溶液呈中性。
【猜想与假设】
①氢氧化钠没有变质;②该氢氧化钠部分变质;③该氢氧化钠 。
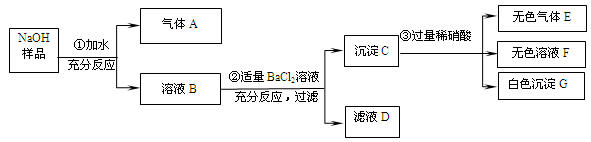
【设计实验】取氢氧化钠固体样品溶于水配成溶液A,进行如下实验:
| 实验步骤 | 实验现象 | 结论及解释 |
| (1)取少量溶液A于试管中,向其中滴加足量的稀盐酸; | 有气泡产生 | 猜想 不成立 |
| (2)另取少量溶液A于试管中,向其中滴加足量的氯化钙溶液; | 产生 | 反应的化学方程式为: |
| (3)将步骤(2)所得的混合液静置,向上层清液中滴加无色的酚酞溶液。 | 溶液呈红色 | 猜想 成立 |
【反思与交流】
久置的氢氧化钠变质的原因是(用化学方程式表示) ,因此,氢氧化钠应 保存。
【探索与拓展】为进一步探究氢氧化钠的变质程度,小明称取18.6g氢氧化钠固体样品放入烧杯中,向其中逐滴加入稀盐酸,到不再产生气泡为止,共消耗稀盐酸100g,反应后称得烧杯中溶液的质量为114.2g。试计算:
(1)该样品中碳酸钠的质量为 ;
(2)该氢氧化钠的变质程度(即变质的氢氧化钠占变质前的氢氧化钠的质量分数)为 。
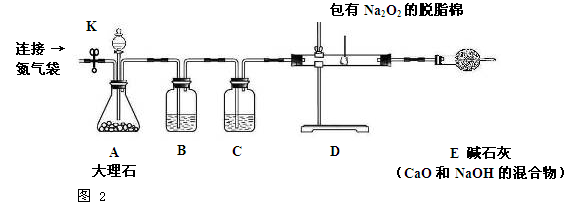
学完酸碱盐知识后,小美对妈妈焙制糕点用的小苏打很感兴趣,她把小苏打带到实验室与小刚一起进行探究.
(1)小美取少量小苏打溶于水,滴加酚酞试液后,溶液变红,说明小苏打的水溶液显 性;
(2)小刚在烧杯内放入少量小苏打,向其中滴加稀盐酸,立即有 产生,说明小苏打能与酸反应.在医疗上可以用小苏打治疗 ;
(3)小美想:糕点非常松软,是不是小苏打受热分解产生了CO2气体呢?于是她如图装置对小苏打进行加热,一段时间后,导管口的确有气泡冒出,澄清石灰水变浑浊,同时试管口有水珠生成.当导管口不再有气泡产生时,试管内仍有白色固体,她猜测剩余固体可能是:①NaOH;②Na2CO3;③NaCl.小刚认为猜想 一定不正确,理由是 .小刚从试管内取少量白色固体溶于水,滴加酚酞,溶液变红,他判断该固体为NaOH,小美认为他的实验设计不合理,因为 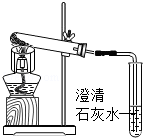
(4)小美和小刚继续探究固体成分,设计了如下实验:
| 操作步骤 | 实验现象 | 结论 |
| 取少量白色固体于试管中,加水溶解,向其中滴加 溶液 | 产生白色沉淀 | 试管内剩余的固体为Na2CO3 |
通过实验证明小苏打受热会分解,反应的化学方程式为: .通过本次探究学习,小美对小苏打的性质有了全面的认识,她给妈妈提出保存小苏打的建议有: (答出一点即可).
碳酸氢钠常用于食品和医药工业,某化学兴趣小组对碳酸氢钠进行探究。
【查阅资料】 Ⅰ.碳酸氢钠受热容易分解,生成水、二氧化碳气体和一种常见的固体物质。
Ⅱ.碳酸钠溶液呈碱性。
【进行实验】为了验证碳酸氢钠受热时会分解,兴趣小组的同学取一定质量的碳酸氢钠到铜片上加热,如图所示。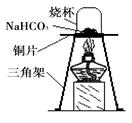
(1)加热一段时间后,观察到烧杯内壁有__________。
(2)充分加热后,将烧杯迅速倒转过来,倒入适量的澄清石灰水,振荡,观察到石灰水变浑浊。写出该反应的化学方程式:___________________。
(3)兴趣小组的同学认为:充分加热后的固体产物可能是NaOH或Na2CO3。
①他们的依据是____________________________________。
②兴趣小组为了确定反应后的固体产物成分进行以下实验,请填写下表:
| 实验 | 实验现象 | 结论 |
| 实验一:取少量反应后的固体产物溶于水,滴入几滴酚酞试液 | 溶液变成红色 | 固体产物是NaOH,而不是Na2CO3 |
| 实验二:取少量反应后的固体产物溶于水,加入氯化钙溶液 | _____________ | 固体产物是Na2CO3,而不是NaOH |
| 实验三:___________________ ___________________________ | 产生大量气泡 | 固体产物是Na2CO3,而不是NaOH |
【讨论与评价】实验一的结论与实验二、实验三的结论相反,在讨论时兴趣小组的同学认为方案一的结论不正确,他们的理由是_____________________________________________。
【总结】请写出碳酸氢钠受热分解的化学方程式________________________。
(4)某碱厂的主要产品之一是小苏打(碳酸氢钠),为了测定产品中碳酸氢钠的质量分数(假设该样品中只含氯化钠一种杂质),取样品10.0 g逐滴加入稀盐酸,所得气体的质量为4.4 g。求:样品中碳酸氢钠的质量分数。