题目内容
【题目】水和溶液在生产生活中起着重要的作用。
(1)海水中含量最多的物质是___________________。
(2)下列做法有利于保护水资源的是___(填序号)。
A.大量使用化肥、农药 B.工业废水处理达标后排放
C.使用含磷洗衣粉 D.生活污水直接排放
(3)生活中,一般可用________的方法来使硬水转化为软水。
(4)我国研制出比漂白粉更高效的饮用水消毒剂“ClO2”,完成制取 ClO2 的反应的化学方程式: Cl2 + 2NaClO2=2ClO2 +_________。
(5)KNO3 和 NaCl 的溶解度曲线如图甲,20℃时取 18g KNO3和 18gNaCl 分别放入两只烧杯中,各加入 50mL水(水的密度 1g/mL),充分溶解,现象如图乙所示;升温到 50℃时,现象如图丙所示。请回答下列问题:
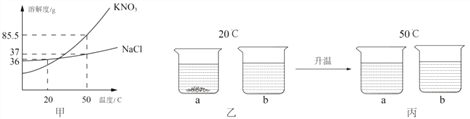
①乙图中,a 烧杯溶液中溶质的质量分数 ___________________b 烧杯溶液中溶质的质量分数(选填“>” “<”或“=”)。
②要使丙图中的 NaCl 溶液恰好变成饱和溶液,需要加入 ___________________ gNaCl 固体。
③除去固体 KNO3中混有的少量 NaCl,实验步骤:先加水加热溶解,再 ___________________ ,然后过滤、洗涤、干燥。
【答案】H2O B 煮沸 2NaCl < 0.5g 降温
【解析】
本题考查了海水的成分、水的污染、硬水的转化、质量守恒定律、溶解度曲线及其应用等。
(1)海水中含量最多的物质是H2O;
(2)A、大量使用化肥、农药时农作物消耗不了的化肥和农药会污染水源和空气,错误;B、工业废水经处理后,减少了对水的污染,正确;C、含磷洗衣粉以磷酸盐作为主要助剂,磷酸盐是一种高效助洗剂,同时也是藻类的助长剂,水中的磷含量升高,水质趋向富营养化,会导致各种藻类、水草大量滋生,水体缺氧会使鱼类死亡等现象;错误;D、生活污水主要是城市生活中使用的各种洗涤剂和污水、垃圾、粪便等,多为无毒的无机盐类,生活污水 中含氮、磷、硫多,致病细菌多,直接排放会污染水,错误。故选B;
(3)生活中,一般可用煮沸的方法来使硬水转化为软水;
(4)根据质量守恒定律可知,反应物中有6个氯原子、2个钠原子、4个氧原子,生成物中有4个氯原子,2个氧原子,只少了2个氯原子,2个钠原子,所以另一种生成物是氯化钠,制取 ClO2 的反应的化学方程式是,Cl2+2NaClO2═2ClO2+2NaCl;
(5)①乙图中,a固体有剩余,b固体全部溶解,a烧杯溶液中溶质的质量分数小于b烧杯溶液中溶质的质量分数;
②50℃时氯化钠的溶解度为37g,50℃时100g水中溶解37g氯化钠达到饱和,图中烧杯中的水的质量为50g,溶解18.5g的氯化钠达到饱和,要使丙图中的NaCl溶液恰好变成饱和溶液,需要加入(18.5g-18g)=0.5gNaCl固体;
③KNO3的溶解度随温度的降低而降低且受温度影响较大。除去固体KNO3中混有的少量NaCl,实验步骤:先加水加热溶解,再降温,然后过滤、洗涤、干燥。