题目内容
(1)(6分)“假酒”中含有一定量的甲醇(化学式为CH3OH),饮用后会使人视力迅速下降、失明,甚至死亡。请回答:
① 甲醇的相对分子质量为 。
② 甲醇中C、H、O三种元素的质量比为 。
③ 甲醇中氧元素的质量分数为 。
(2)(10分)实验室可用加热氯酸钾与二氧化锰的混合物制取氧气,其反应的化学方程式为:2KClO3 2KCl + 3O2↑。现加热氯酸钾与二氧化锰的混合物30g,待氯酸钾完全反应后,称得剩余固体的质量为20.4g。求:
2KCl + 3O2↑。现加热氯酸钾与二氧化锰的混合物30g,待氯酸钾完全反应后,称得剩余固体的质量为20.4g。求:
① 反应生成氧气的质量是多少?
② 原混合物中氯酸钾的质量是多少?
① 甲醇的相对分子质量为 。
② 甲醇中C、H、O三种元素的质量比为 。
③ 甲醇中氧元素的质量分数为 。
(2)(10分)实验室可用加热氯酸钾与二氧化锰的混合物制取氧气,其反应的化学方程式为:2KClO3
 2KCl + 3O2↑。现加热氯酸钾与二氧化锰的混合物30g,待氯酸钾完全反应后,称得剩余固体的质量为20.4g。求:
2KCl + 3O2↑。现加热氯酸钾与二氧化锰的混合物30g,待氯酸钾完全反应后,称得剩余固体的质量为20.4g。求:① 反应生成氧气的质量是多少?
② 原混合物中氯酸钾的质量是多少?
(1)(6分)①32 ② 3∶1∶4 ③ 50%
(2)(8分)① 9.6g ② 24.5g
(2)(8分)① 9.6g ② 24.5g
试题分析:(1)由甲醇(化学式为CH3OH)的化学式可知:
① 甲醇的相对分子质量为12+1×4+16=32。
② 甲醇中C、H、O三种元素的质量比为12:1×4:16=3∶1∶4。
③ 甲醇中氧元素的质量分数为
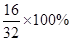 =50%。
=50%。(2)由题意得:
① 反应生成氧气的质量为:30g-20.4g=9.6g。
②设原混合物中氯酸钾的质量为x
2KClO3
 2KCl + 3O2↑
2KCl + 3O2↑245 96
x 9.6g
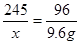
解得:x=24.5g
答案:原混合物中氯酸钾的质量为24.5g。
点评:本题集中考查了跟化学式、化学方程式有关的计算,难度较大。
化合物的相对分子质量等于化合物中各元素相对原子质量的总和;
化合物中各元素的质量比等于各元素相对原子质量与原子个数乘积的比。
某元素的质量分数=
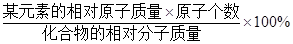 。
。根据化学方程式计算,要注意解题的步骤,设、写、找、列、解、答。

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案
相关题目