题目内容
(8分)某化学兴趣小组为了测定某石灰石样品中碳酸钙的质量分数,取用2.0 g石灰石样品,把25.0g质量分数为10%的稀盐酸分五次加入样品中(样品中的杂质既不与盐酸反应,也不溶解于水),每次充分反应后都经过滤、干燥、称量,得实验数据如下:
请计算:
(1)2.0g石灰石样品中碳酸钙的质量为 ,石灰石中碳酸钙的质量分数为 。
(2)请你继续计算反应生成溶液中氯化钙的质量分数(计算过程和结果均保留一位小数)。
| 实验次数 | 1 | 2 | 3 | 4 | 5 |
| 稀盐酸的累计加入量 | 5.0g | 10.0g | 15.0g | 20.0g | 25.0 g |
| 剩余固体的质量 | 1.5g | 1.0g | 0.5g | 0.3g | 0.3g |
(1)2.0g石灰石样品中碳酸钙的质量为 ,石灰石中碳酸钙的质量分数为 。
(2)请你继续计算反应生成溶液中氯化钙的质量分数(计算过程和结果均保留一位小数)。
(1)1.7g 85% (2)7.3%
试题分析:(1)根据题意,反应剩余的固体的质量,即是杂质的质量,再由杂质的质量可计算出石灰石中碳酸钙的质量,从而由碳酸钙的质量可计算出石灰石中碳酸钙的质量分数。根据表格中的数据分析可知,最后剩余的0.3g为杂质质量,所以石灰石中碳酸钙的质量为2.0g-0.3g=1.7g,则石灰石中碳酸钙的质量分数为
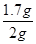 ×100%=85%。
×100%=85%。(2)由碳酸钙的质量,结合化学方程式,可计算出生成的氯化钙的质量和二氧化碳的质量,进而计算出生成溶液中氯化钙的质量分数。
设反应生成CaCl2的质量为x,CO2的质量为y 。
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 111 44
1.7g x y
 解得,x=1.9g
解得,x=1.9g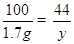 解得,y=0.7g
解得,y=0.7g则反应后所得溶液的质量=1.7g+25g-0.7g=26g
所以,反应后的氯化钙的溶质质量分数=
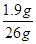 ×100%=7.3%。
×100%=7.3%。 答:反应后生成的溶液中氯化钙的溶质质量分数为7.3% 。
点评:此题是关于化学方程式及溶质质量分数的计算题,要求学生要有较强的分析能力和数据处理能力;解题的关键是,要会利用化学反应,并结合表格中的数据分析判断出杂质的质量(这是本题所隐藏的关键条件),从而判断出样品中碳酸钙的质量;然后再根据相关的化学反应方程式,并依据已知量对未知的应求量进行求解计算即可,注意解题要规范。

练习册系列答案
 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案
相关题目


 2KCl + 3O2↑。现加热氯酸钾与二氧化锰的混合物30g,待氯酸钾完全反应后,称得剩余固体的质量为20.4g。求:
2KCl + 3O2↑。现加热氯酸钾与二氧化锰的混合物30g,待氯酸钾完全反应后,称得剩余固体的质量为20.4g。求: CaO+CO2↑,将100 g含CaCO3质量分数为80 %的石灰石样品(杂质不发生反应,也不含钙元素),高温煅烧一段时间后,冷却,测得剩余固体中含钙元素的质量分数为41%,则生成的CaO的质量约为
CaO+CO2↑,将100 g含CaCO3质量分数为80 %的石灰石样品(杂质不发生反应,也不含钙元素),高温煅烧一段时间后,冷却,测得剩余固体中含钙元素的质量分数为41%,则生成的CaO的质量约为 Si + 4HCl。若要制得14g硅,参加反应的氢气质量是多少克?
Si + 4HCl。若要制得14g硅,参加反应的氢气质量是多少克?