题目内容
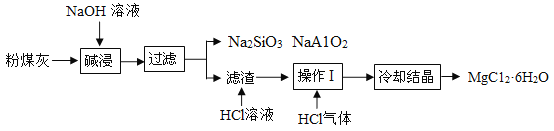
【题目】某金属冶炼厂的管道烟泥中含有Cu、Zn及炭黑,现欲回收铜和锌,主要流程如图所示:
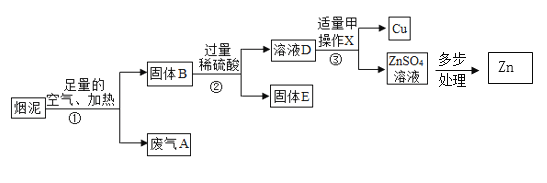
(1)溶液D中一定含有的溶质是_____。
(2)步骤③中发生反应的一个化学方程式是_____。
(3)步骤②中参加反应的物质有ZnO和_____。
(4)有人认为若步骤①中空气不足量,会导致锌的回收率降低,说出你认为的看法并说明理由_____。
【答案】CuSO4、ZnSO4、H2SO4 Zn+H2SO4═ZnSO4+H2↑或Zn+CuSO4=ZnSO4+Cu CuO 不正确,不管锌在第一步中是否被氧化,在第二步中都会完全转化为硫酸锌,不会影响锌的回收
【解析】
根据给出的转化关系对应的过程分析每个对应的问题,或者直接分析每个问题,从给出的信息中找对应的信息。
(1)由于固体时含锌和铜,且加入的硫酸过量,所以溶液D中一定含有的溶质是 生成的CuSO4和ZnSO4以及过量的H2SO4。
(2)步骤③中加入的是锌,所以发生反应为锌和硫酸铜以及硫酸反应,对应的化学方程式是 Zn+H2SO4═ZnSO4+H2↑或Zn+CuSO4=ZnSO4+Cu。
(3)步骤②中根据铜锌和氧气反应生成氧化锌和氧化铜,可知参加反应的物质为ZnO和 CuO。
(4)有人认为若步骤①中空气不足量,会导致锌的回收率降低,不正确。理由:不管锌在第一步中是否被氧化,在第二步中都会完全转化为硫酸锌,不会影响锌的回收。

 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案【题目】氢化钙(CaH2)固体是登山运动员常用的能源提供剂。某化学兴趣小组在实验室模拟制备氢化钙,并用制得的氢化钙进行实验探究。
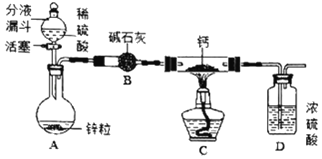
实验一:实验室模拟制备氢化钙
(查阅资料)①用H2与钙加热的方法可制得CaH2
②钙遇水立即发生剧烈反应生成氢氧化钙和氢气
③碱石灰能吸收水蒸气
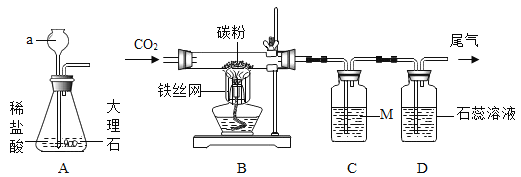
同学们设计了如图所示的实验装置。
(1)写出装置A中反应的化学方程式_____。
(2)装置D的作用是_____。
(3)制得的氢化钙要密封保存,其遇水反应生成一种碱和一种可燃性气体,写出该反应的化学方程式_____。
实验二:取少量上述制得的CaH2样品加入到一定量的碳酸钠溶液中,产生大量气泡,过滤,得到滤渣和滤液。经检验滤渣的成分是碳酸钙,小组同学对滤液的溶质进行探究
(猜想假设)猜想一:NaOH 猜想二:NaOH、Ca(OH)2
猜想三:NaOH、Na2CO3 猜想四:NaOH、Na2CO3、Ca(OH)2
经过讨论,大家一致认为猜想四不合理,原因是_____。
(实验验证)
实验操作 | 实验现象 | 实验结论 |
1、取滤液,向其中滴入少量的Na2CO3溶液 | _____ | 猜想二不成立 |
2、另取滤液,向其中加入足量的稀盐酸 | _____ | 猜想三成立 |
(拓展延伸)
登山运动员用氢化钙作能源提供剂,与氢气相比,优点是_____。