题目内容
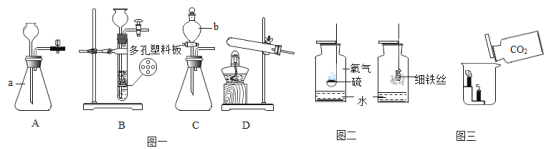
【题目】根据下图所示的实验回答问题。
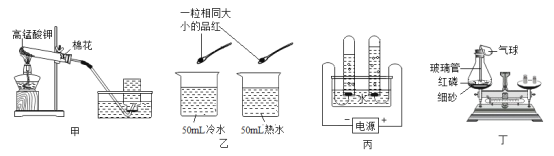
(1) 甲中棉花的作用是_____。
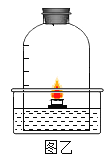
(2) 乙的目的是研究品红分子在水中的运动速率与_____的关系。
(3) 丙是电解水实验,反应的化学方程式为_____;与电源正极相连的试管中产生的气体是_____。
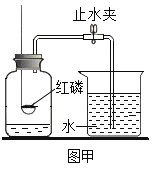
(4) 丁是验证质量守恒定律。其中红磷燃烧的化学方程式为_____;充分反应并冷却后,天平仍保持平衡,从微观的角度解释其原因:_____。
【答案】防止固体粉末进入导管 温度 2H2O 2H2↑+O2↑ 氧气(或O2) 4P+5O2
2H2↑+O2↑ 氧气(或O2) 4P+5O2 2P2O5 化学反应前后原子的种类、数目和质量都不变
2P2O5 化学反应前后原子的种类、数目和质量都不变
【解析】
(1) 甲中棉花的作用是防止固体粉末进入导管;
(2) 乙实验中,温度条件不相同,其他条件相同,其目的是研究品红分子在水中的运动速率与温度的关系
(3) 丙是电解水实验,电解过程中,水分解生成氢气和氧气,反应的化学方程式为2H2O 2H2↑+O2↑;与电源正极相连的试管中产生的气体是氧气(或O2);
2H2↑+O2↑;与电源正极相连的试管中产生的气体是氧气(或O2);
(4)红磷燃烧生成五氧化二磷,反应的化学方程式为4P+5O2 2P2O5;充分反应并冷却后,天平仍保持平衡,从微观的角度解释其原因:化学反应前后原子的种类、数目和质量都不变。
2P2O5;充分反应并冷却后,天平仍保持平衡,从微观的角度解释其原因:化学反应前后原子的种类、数目和质量都不变。

 阅读快车系列答案
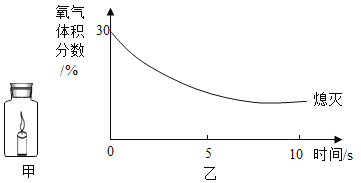
阅读快车系列答案【题目】在利用红磷燃烧测定空气中氧气含量的实验中,用传感器记录集气瓶内氧气浓度随时间变化的情况,如图所示。

(进行实验)
活动1:证明红磷熄灭后,氧气还有剩余
实验装置 | 实验步骤 | 现象 | 结论 |
Ⅰ.用高能激光笔照射燃烧匙中足量的红磷 | 红磷燃烧,放出大量热,一段时间后熄灭,白磷始终不燃烧 | 红磷熄灭后,氧气还有剩余 | |
Ⅱ.冷却后,将装有白磷的燃烧匙提出水面,用高能激光笔照射 | 白磷 现象① |
(解释与结论)
(1)红磷燃烧的化学方程式为______________________。
(2)步骤Ⅰ中白磷始终不燃烧的原因是__________________。
(3)步骤Ⅱ中的现象①是_______________________。
(4)实验中气球的作用是_______________________。
活动2:探究影响剩余氧气浓度的因素
用如图装置进行实验,得到数据如表。
可燃物 | 白磷 | 红磷 | 木炭 |
着火点/℃ | 40 | 240 | 370 |
生成物状态 | 固态 | 固态 | 气态 |
剩余氧气浓度 | 3.1% | 7.0% | 14.0% |

(5)通过对比右表中红磷和白磷的相关数据,可以得出影响剩余氧气浓度的因素可能是________。
(6)结合以上探究及实验数据,在“测定空气中氧气含量”的实验中,通常使用红磷而不用木炭的原因可能有________。
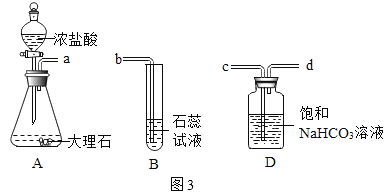
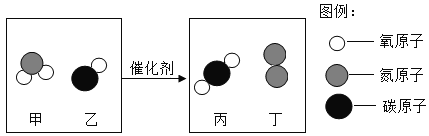
【题目】化学小组用图1装置验证二氧化碳与水的反应。

盐酸浓度 | 观察到的现象 | |
甲组 | 浓盐酸(36.5%) | B中石蕊溶液由紫色变成红色 C中石蕊溶液没有变为紫色 |
乙组 | 稀盐酸(13.5%) | B中石蕊溶液由紫色变为红色 C中石蕊溶液变为紫色 |
(1)A中反应的化学方程式为_____。
(2)乙组C中反应的化学方程式为_____。
(讨论与交流)同学们认为甲组C中石蕊溶液没有变为紫色,是因为浓盐酸挥发出过多的HCl溶于石蕊溶液。
(提出猜想)盐酸的挥发性与浓度有关。
(进行实验)用图2装置研究不同浓度盐酸的挥发性。用离子传感器测定烧杯中所得溶液的氯离子浓度(氯离子浓度可以近似表示挥发出的HCl的量),实验数据见下表。
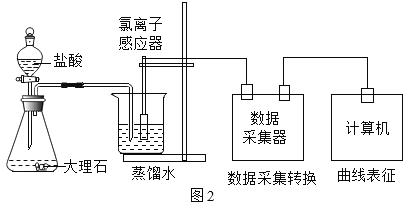
盐酸浓度与氯离子浓度的对应关系(相同时间内测得)
盐酸浓度(%) | 13.5 | 20 | 26.2 | 29.2 | 32.2 | 36.5 |
氯离子浓度(mg/L) | 1.1 | 1.4 | 3.7 | 19.0 | 59.8 | 209.2 |
分析表中数据,能够得出盐酸的挥发性与浓度的关系是_____。
(得出结论)猜想正确
(实验反思)甲组石蕊溶液变红不能证明二氧化碳与水反应。
(实验改进)甲组同学在装置A与装置B之间连接装置D。三个装置之间导管口的连接顺序是:a→_____ →_____→b。选择饱和NaHCO3溶液除杂的原因是_____。