题目内容
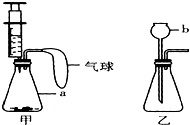 根据如图所示两套装置,请回答:
根据如图所示两套装置,请回答:(1)写出图中标号仪器的名称a
(2)用甲装置进行实验:把注射器内的无色液体推入仪器a中与固体反应,观察到气球胀大.符合该现象的反应有:
①分解反应:
②化合反应:CaO+H2O═Ca(OH)2,气球胀大的原因是
③其他反应:若仪器a中的固体是Mg粉或Na2CO3粉末,则注射器中的液体可以是
(3)乙装置中用注射器代替仪器b后,用于实验室制气体,其优点是
考点:反应现象和本质的联系,常用气体的发生装置和收集装置与选取方法,生石灰的性质与用途,酸的化学性质,书写化学方程式、文字表达式、电离方程式
专题:实验性简答题
分析:(1)根据常见仪器的名称进行解答;
(2)根据甲装置适用于固体和液体混合反应不需要加热的反应、氧化钙和水反应生成氢氧化钙放出大量的热以及Mg粉或NaHCO3粉末与酸反应放出氢气或二氧化碳进行解答;
(3)根据乙装置中用注射器代替仪器b后其优点是易于控制滴入试剂的量以控制反应速率进行解答.
(2)根据甲装置适用于固体和液体混合反应不需要加热的反应、氧化钙和水反应生成氢氧化钙放出大量的热以及Mg粉或NaHCO3粉末与酸反应放出氢气或二氧化碳进行解答;
(3)根据乙装置中用注射器代替仪器b后其优点是易于控制滴入试剂的量以控制反应速率进行解答.
解答:解:(1)图中标号仪器的名称a:锥形瓶,b:长颈漏斗;
(2)①甲装置适用于固体和液体混合反应不需要加热的反应,分解反应有过氧化氢和二氧化锰混合制取氧气,化学方程式为:2H2O2
2H2O+O2↑;
②氧化钙和水反应生成氢氧化钙放出大量的热,使瓶内气体体积膨胀;
③Mg粉或NaHCO3粉末与酸反应放出氢气或二氧化碳;
(3)乙装置中用注射器代替仪器b后其优点是易于控制滴入试剂的量以控制反应速率.若让正在发生的反应停止进行,正确的操作方法关闭弹簧夹,这样生成的气体排不出去,使试管内的气压增大,把稀盐酸压回长颈漏斗,使反应物分离开,反应就停止了.
故答案为:(1)锥形瓶;长颈漏斗;
(2)①2H2O2
2H2O+O2↑;
②氧化钙与水反应放出大量的热,使瓶内气体体积膨胀;
③硫酸;
(3)易于控制滴入试剂的量以控制反应速率;关闭弹簧夹.
(2)①甲装置适用于固体和液体混合反应不需要加热的反应,分解反应有过氧化氢和二氧化锰混合制取氧气,化学方程式为:2H2O2
| ||
②氧化钙和水反应生成氢氧化钙放出大量的热,使瓶内气体体积膨胀;
③Mg粉或NaHCO3粉末与酸反应放出氢气或二氧化碳;
(3)乙装置中用注射器代替仪器b后其优点是易于控制滴入试剂的量以控制反应速率.若让正在发生的反应停止进行,正确的操作方法关闭弹簧夹,这样生成的气体排不出去,使试管内的气压增大,把稀盐酸压回长颈漏斗,使反应物分离开,反应就停止了.
故答案为:(1)锥形瓶;长颈漏斗;
(2)①2H2O2
| ||
②氧化钙与水反应放出大量的热,使瓶内气体体积膨胀;
③硫酸;
(3)易于控制滴入试剂的量以控制反应速率;关闭弹簧夹.
点评:气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案
相关题目
2011年被联合国定为“国际化学年”,以纪念化学所取得的成就以及对人类文明的贡献,下列体现化学造福人类的是( )


| A、(1)(3) |
| B、(1)(2)(4) |
| C、(1)(3)(4) |
| D、(1)(2)(3)(4) |
 (1)如表列出了氯化铵在不同温度下的溶解度.
(1)如表列出了氯化铵在不同温度下的溶解度.