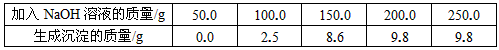
题目内容
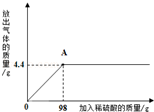
某课外活动小组为测定当地石灰石中含碳酸钙的质量分数,取来了一些矿石,准确称取25g放于盛有200g稀盐酸(氯化氢的水溶液)的烧杯中(杂质不溶于水,也不与稀盐酸反应,也不分解),恰好完全反应。测得烧杯内物质的总质量与时间的关系如图所示(溶解的气体忽略不计)。
试计算:
(1)生成二氧化碳的质量是 _;
(2)所用稀盐酸的溶质质量分数是多少?
(3)石灰石中碳酸钙的质量分数是多少?
(1)8.8g;(2)7.3%;(3)80%
解析试题分析:(1)生成二氧化碳的质量是8.8g;
(2)解:设稀盐酸中的溶质质量为X,石灰石中碳酸钙质量为Y
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 73 44
Y X 8.8g
8.8g︰44 = X︰73 = Y︰100
X = 14.6g Y = 20g
所用稀盐酸的溶质质量分数="14.6g/200g" x 100% ="7.3%"
(3)石灰石中碳酸钙的质量分数=" 20g/25g" x 100% =80%)
答:所用稀盐酸的溶质质量分数为7.3%;石灰石中碳酸钙的质量分数为80%。
考点:质量守恒定律、化学方程式的计算、质量分数的计算

练习册系列答案
相关题目