题目内容
28g石灰石样品与210.8g稀盐酸恰好完全反应后(样品中的杂质既难溶于水,又不与稀盐酸反应),生成了8.8g二氧化碳。(溶解在水中的二氧化碳忽略不计)计算:
(1)该石灰石样品中碳酸钙的质量分数。
(2)所得溶液的溶质质量分数。
解析试题分析:
解:(1)设碳酸钙的质量为x,反应生成氯化钙的质量为y,
CaCO3+2HCl═CaCl2+H2O+CO2↑,
100 111 44
x y 8.8g
100:44=x:8.8g 111:44=y:8.8g
x=20g,y=22.2g,
该石灰石样品中碳酸钙的质量分数为: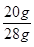 ×100%=71.4%;
×100%=71.4%;
答:石灰石样品中碳酸钙的质量分数为71.4%.
(2)氯化钙溶液的质量为:20g+210.8g-8.8g=222g,
所得氯化钙溶液的质量分数为: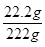 ×100%=10%;
×100%=10%;
答:所得氯化钙溶液的质量分数为10%.
考点:根据化学方程式的计算、溶质质量分数的计算

练习册系列答案
 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案
相关题目
现有铜与另一种金属的混合物粉末,另一种金属可能是镁、铁、锌中的一种,现欲测定其组成.
【查阅资料】(1)镁、铁、锌皆能与稀硫酸发生置换反应,且生成+2价的可溶性金属硫酸盐和氢气.
(2)相对原子质量:Mg﹣24、Fe﹣56、Zn﹣65
【实验步骤及数据】取该混合物粉末8.0g放入烧杯中,将140.0g 14.0%的稀硫酸分四次加入该烧杯中,充分反应后,测得剩余固体质量数据记录如下:
| 次数 | 1 | 2 | 3 | 4 |
| 加入稀硫酸的质量/g | 35.O | 35.0 | 35.O | 35.O |
| 剩余固体的质量/g | 6.8 | 5.6 | 4.4 | 4.2 |
通过计算(写出计算过程),求:
(1)该混合物粉末中铜的质量分数?
(2)该混合物粉末中另一金属为何种金属?
(3)第三次加入硫酸充分反应后,所得溶液中溶质的质量分数是多少?