题目内容
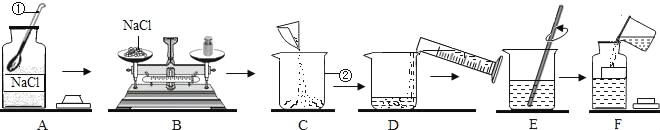
【题目】请根据下列装置图,回答有关问题:

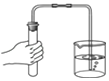
(1)写出图中标号仪器的名称:①__________;
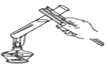
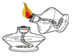
(2)实验室用高锰酸钾制氧气,发生装置应选____,实验时,需对该装置做一点改动_。写出用高锰酸钾制氧气的化学方程式___________________;若用F 装置收集氧气,如何验满?______________________________________________
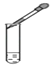
(3)用C装置代替B装置制取氢气的优点是_______________;写出实验室制氢气的化学方程式 _______________________________;
(4)亚硝酸钠是实验室常用的试剂,实验室一般用亚硝酸钠溶液与氯化铵溶液反应来制取N2。N2的化学性质十分稳定,但在一定条件下能与H2部分化合生成NH3。下图为制取少量NH3的装置(制取H2的装置已略去)。
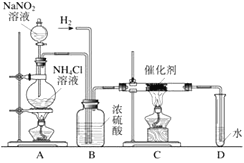
①C装置的硬质试管中发生反应的化学方程式为________________________。
②反应时N2和H2的最佳质量比是_________。如果按此比例进行反应,反应时,若D中导管口有气泡逸出,(已知NH3极易溶于水),说明逸出气泡的原因__________________。
③用实验方法证明确实有NH3生成: ________________________________。
【答案】长颈漏斗 A 在试管口放一团棉花 2KMnO4![]() K2MnO4 + MnO2 + O2↑ 在b端管口放一根带火星的木条,木条复燃,证明氧气满了 可以控制反应的发生和停止 Zn+H2SO4=ZnSO4+H2↑ N2+3H2
K2MnO4 + MnO2 + O2↑ 在b端管口放一根带火星的木条,木条复燃,证明氧气满了 可以控制反应的发生和停止 Zn+H2SO4=ZnSO4+H2↑ N2+3H2 ![]() 2NH3 14:3 氮气和氢气部分化合,仍会有未反应的H2和N2逸出 把湿润的红色石蕊试纸放在导管口,红色变蓝色,证明生成氨气
2NH3 14:3 氮气和氢气部分化合,仍会有未反应的H2和N2逸出 把湿润的红色石蕊试纸放在导管口,红色变蓝色,证明生成氨气
【解析】
(1)图中标号仪器的名称为:长颈漏斗;
(2)用高锰酸钾制氧气时,反应物的状态是固体,反应条件是加热,发生装置应选A;为防止高锰酸钾进入导气管,需在试管口放一团棉花,对该装置做一点改动是在试管口放一团棉花;高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,反应的化学方程式为:2KMnO4![]() K2MnO4 + MnO2 + O2↑;氧气的密度大于空气,若用F装置收集氧气,气体需从a管通入,氧气具有助燃性,能使带火星的木条复燃。氧气验满的方法是:在b端管口放一根带火星的木条,木条复燃,证明氧气满了;
K2MnO4 + MnO2 + O2↑;氧气的密度大于空气,若用F装置收集氧气,气体需从a管通入,氧气具有助燃性,能使带火星的木条复燃。氧气验满的方法是:在b端管口放一根带火星的木条,木条复燃,证明氧气满了;
(3)在装置C中,固体药品物放在多孔隔板上,液体药品从长颈漏斗中加入。关闭开关时,试管中的气体增多,压强增大,把液体压入长颈漏斗,固体和液体分离,反应停止,打开开关时,气体导出,试管中的气体减少,压强减小,液体和固体混合,反应进行。用C装置代替B装置制取氢气的优点是:可以控制反应的发生和停止;锌和硫酸反应生成硫酸锌和氢气反应的化学方程式为:Zn+H2SO4=ZnSO4+H2↑;
(4)①N2的化学性质十分稳定,但在一定条件下能与H2部分化合生成NH3,反应的化学方程式为:N2+3H2 ![]() 2NH3;
2NH3;
②根据化学方程式N2+3H2 ![]() 2NH3可知,反应时N2和H2的最佳质量比=28:6=14:3,若D中导管口有气泡逸出,是因为氮气和氢气部分化合,仍会有未反应的H2和N2逸出;
2NH3可知,反应时N2和H2的最佳质量比=28:6=14:3,若D中导管口有气泡逸出,是因为氮气和氢气部分化合,仍会有未反应的H2和N2逸出;
③氨气溶于水呈碱性,红色石蕊试纸遇碱性物质变蓝色。用实验方法证明确实有NH3生成:把湿润的红色石蕊试纸放在导管口,红色变蓝色,证明生成氨气。

【题目】溶液是生产生活中常见的物质,依据相关信息回答问题:
资料:硝酸钾的溶解度数据(部分数据已做取整数处理)如下表所示:
温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
溶解度/g | 21 | 32 | 46 | 64 | 86 | 110 | 138 |
(1)农业上,硝酸钾用作水溶性肥料,硝酸钾溶液中的溶质是_____。
(2)A、B、C、D四个烧杯中分别盛有100g水,在40℃时,向四个烧杯中分别加入110g、86g、64g、32g硝酸钾,充分溶解,如图所示。
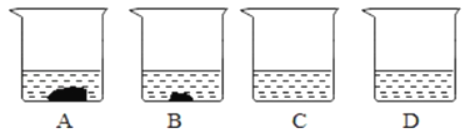
①_____(填字母序号)中盛的一定是饱和溶液。
②使B烧杯的溶液升温至50℃时,溶液的质量为_____g。
③采用一种方法使A中的固体恰好溶解。对于最终四个烧杯中的溶液,下列说法正确的是_____(填字母序号)。
A 溶剂质量可能相等 B 溶质质量可能相等
C 溶质质量分数可能有相等的 D 烧杯A中的溶液质量分数可能最大