题目内容
【题目】质量守恒定律的定量研究对化学科学发展具有重大意义。
(1)下图为某化学反应的微观模拟图,“○”和“●”分别表示两种不同的原子:
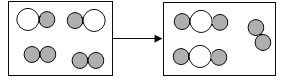
由“![]() ”聚集成的物质______(填“可能”或“不可能”)是氧化物,参加反应的两种反应物的分子个数比为 _____,此反应的基本反应类型为______。请写出一个符合上述反应的化学方程式_____。
”聚集成的物质______(填“可能”或“不可能”)是氧化物,参加反应的两种反应物的分子个数比为 _____,此反应的基本反应类型为______。请写出一个符合上述反应的化学方程式_____。
(2)已知m1g镁条放在空气中完全燃烧,生成m2g氧化镁(不考虑其它反应),则m1______m2。 小西在做该实验时,观察到耀眼的白光,冒出大量白烟,称量无误时,发现m1>m2,其原因是______。
【答案】可能 1:2(或2:1) 化合反应 2CO+O2![]() 2CO2 小于 生成物氧化镁部分以白烟的形式逸散(或扩散)到空气中
2CO2 小于 生成物氧化镁部分以白烟的形式逸散(或扩散)到空气中
【解析】
(1)将图中前后无变化的微粒去除得图:
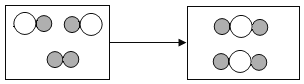
图示表示 由“![]() ”聚集成的物质由两种元素组成,可能一种为氧元素,所以该物质可能为氧化物;每1个反应物分子和2个另一种反应物分子反应,两种反应物分子个数比为1:2(或2:1);该反应的反应物是两种,生成物是一种,属于化合反应;符合图的方程式为:2CO+O2
”聚集成的物质由两种元素组成,可能一种为氧元素,所以该物质可能为氧化物;每1个反应物分子和2个另一种反应物分子反应,两种反应物分子个数比为1:2(或2:1);该反应的反应物是两种,生成物是一种,属于化合反应;符合图的方程式为:2CO+O2![]() 2CO2;故填:可能;1:2(或2:1);化合反应;2CO+O2
2CO2;故填:可能;1:2(或2:1);化合反应;2CO+O2![]() 2CO2
2CO2
(2)根据质量守恒定律,生成氧化镁的质量=参加反应的镁的质量+氧气的质量,所以m1小于m2;镁带燃烧时放出耀眼的白光,放出大量的热,放出大量的白烟,生成物氧化镁部分以白烟的形式逸散(或扩散)到空气中,使m1>m2。故填:小于;生成物氧化镁部分以白烟的形式逸散(或扩散)到空气中

 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案【题目】我市某地石灰石资源丰富,化学兴趣小组的同学为了测定该石灰石中碳酸钙的质量分数,用托盘天平称取了5份石灰石样品,分别加入各盛有200.0克稀盐酸的烧杯中充分反应(假设杂质不反应),得如下实验数据:
实验编号 | 1 | 2 | 3 | 4 | 5 |
石灰石样品的质量/g | 12.5 | 25.0 | 37.5 | 50.0 | 62.5 |
生成CO2的质量/g | 4.4 | 7.5 | 13.2 | 17.6 | 17.6 |
分析上述实验数据并回答:
(1)实验编号为_______的实验数据有明显错误。
(2)这种石灰石样品中碳酸钙的质量分数为__________。
(3)求稀盐酸的溶质质量分数(写出计算过程,结果精确到0.1%)________。