题目内容
【题目】镁条在空气中久置表面会变黑。某小组同学设计并进行实验,探究镁条变黑的条件。
【查阅资料】常温下,亚硫酸钠(Na2SO3)可与O2发生化合反应。
【猜想与假设】常温下,镁条变黑可能与O2、CO2、水蒸气有关。
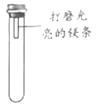
【进行实验】通过控制与镁条接触的物质,利用右图装置(镁条长度为3cm,试管容积为20mL),分别进行下列5个实验,并持续观察20天。
编号 | 主要实验操作 | 实验现象 |
1 | 先充满用NaOH浓溶液洗涤过的空气 再加入2mL浓硫酸 | 镁条始终无明显变化 |
2 | 加入2mL NaOH浓溶液 | 镁条始终无明显变化 |
3 | 先加入2mL浓硫酸 再通入约4mL CO2 | 镁条始终无明显变化 |
4 | 先加入4mL饱和Na2SO3溶液 再充满CO2 | 镁条始终无明显变化 |
5 | 先加入2mL蒸馏水 再通入约4mL CO2 | 镁条第3天开始变黑 至第20天全部变黑 |
【解释与结论】
(1)实验1和2中,NaOH浓溶液的作用是____________(用化学方程式表示)。
(2)实验1的目的是____________。
(3)实验3中,试管内的气体主要含有CO2、__________。
(4)得出“镁条变黑一定与CO2有关”结论,依据的两个实验是___________(填编号)。
(5)由上述实验可推知,镁条变黑的条件是___________。
【反思与评价】
(6)在猜想与假设时,同学们认为镁条变黑与N2无关,其理由是__________。
(7)欲进一步证明镁条表面的黑色物质中含有碳酸盐,所需要的试剂是__________。
【定量分析】小陆同学取了实验室存放较久的1克镁条和20克稀硫酸(足量)放入一支质量为30克的试管中,看到产生较多气泡,等没有气泡后精确称量,得到试管和内容物总质量为50.92克,小陆同学认为此反应产生的全部为氢气。试帮小陆同学计算这1 克镁条中还含有多少镁?
__________
同学们经过讨论一致认为在操作和称量准确的情况下,实际含有的镁要小于计算结果。请你分析可以有原因_____________________________________
【答案】 2NaOH+CO2===Na2CO3+H2O 验证氧气与镁条变黑的关系 氧气,氮气 2,5 镁与氧气,水,二氧化碳接触 氮气化学性质不活泼 稀盐酸和石灰水 0.96克 氢气中混有二氧化碳,水蒸汽等
【解析】(1)实验1和2中,NaOH浓溶液的作用是2NaOH+CO2===Na2CO3+H2O。(2)实验1的目的是验证只有氧气,没有二氧化碳和水时镁条是否会变黑。(3)实验3中,试管内的气体主要含有CO2、氧气,氮气 。(4)得出“镁条变黑一定与CO2有关”结论,依据的两个实验是2,5,两者比较其它条件相同,只有二氧化碳的情况不同,且有二氧化碳的变黑,没有二氧化碳的不变黑,故证明镁条与二氧化碳有关。(5)由上述实验可推知,镁条变黑的条件是镁与氧气,水,二氧化碳接触。(6). 氮气化学性质不活泼,通常不发生化学反应,所以在猜想与假设时,可认为镁条变黑与N2无关 (7). 验证碳酸盐的方法是:将样品中加入适量稀盐酸,如果生成气体,将气体通入澄清石灰水中,澄清石灰水变浑浊,证明样品中有碳酸盐。 (8). 由质量守恒定律可知反应前后物质的总质量不变,所以生成氢气的质量为:1克+20+30克-50.92克=0.08g,设1 克镁条中还含有镁的质量为x,
Mg + H2SO4 == MgSO4 + H2↑
24 2
x 0.08g
24/x=2/0.08g x=0.96克
(9). 镁条表面的黑色物质中含有碳酸盐,加入酸时会生成二氧化碳,所以氢气中混有二氧化碳,水蒸汽等,实际生成氢气的质量小于0.08g,镁的质量小于0.96g。