题目内容
【题目】某化学兴趣小组的同学在进行“活泼金属与酸的反应”实验时,对铝和铝的化合物的性质进行了探究。
[性质探究]
I.金属的活动性
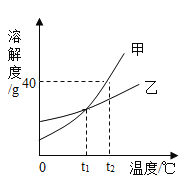
甲同学将用砂纸打磨过的铝片放入氯化镁溶液中,____,说明铝的金属活动性排在镁的________。
II.金属与酸的反应
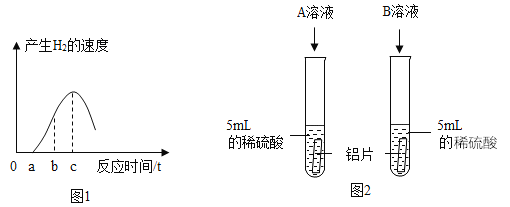
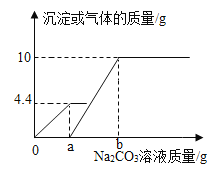
(1)乙同学利用数字传感器测得铝片与稀硫酸反应产生氢气的速度与时间的关系如图1所示,单质铝与稀硫酸反应的化学方程式为__________。图中从0到a这段时间无明显变化的原因是________。
(2)将铝片与浓度相同的足量稀硫酸、稀盐酸反应,结果是生成氢气的速度前者比后者慢很多。丙同学对比盐酸和硫酸的化学式之后,猜想可能是盐酸中的氯离子对反应有促进作用。为了验证是“盐酸中的氯离子对反应有促进作用”的猜想,大家一起设计了如图2所示的实验。如果该实验能证明猜想,加入的B溶液是Na2SO4溶液,依据控制变量的原则,A溶液是_____溶液。
(3)你认为还有可能是___________因素造成的。
【答案】无现象 后面 2Al+3 H2SO4═Al2(SO4)3+3H2↑ 铝表面有氧化铝,氧化铝和酸反应不产生气体 NaCl 硫酸根离子对反应有抑制作用
【解析】
[性质探究](1)甲同学将用砂纸打磨过的铝片放入氯化镁溶液中,观察不到明显的现象,说明铝的金属活动性排在镁的后面;
(1)铝片与稀硫酸反应产生氢气和硫酸铝,反应的化学方程式为2Al+3 H2SO4═Al2(SO4)3+3H2↑;图中0到a这段时间无明显变化,是因为铝表面有氧化铝,一开始是氧化铝和酸反应不产生气体;
(2)为了验证是“盐酸中的氯离子对反应产生促进作用”的猜想,加入的两种溶液一种含氯离子,一种含硫酸根离子,其余相同,则加入的两种溶液是氯化钠或硫酸钠;
(3)使用的还有硫酸,氯离子有促进作用,还可能是硫酸根离子对反应有抑制作用。

 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案【题目】根据图示回答相关问题。
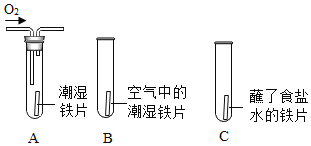
(1)下列通过对照实验探究影响铁生锈的因素。
实验 | 分析 |
| 一段时间后发现A、C 中铁片变红,B中铁片依然光亮,对比A、B中的现象,说明决定铁生锈快慢的一个重要因素是___________;对比B、C中的现象,说明铁生锈快慢与____________有关。 |
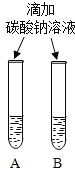
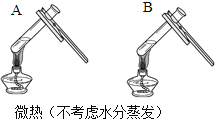
(2)小明同学设计如下两种方案鉴别氢氧化钠和氢氧化钙两种饱和溶液。
实验一 | 实验二 | 分析 |
|
| 两种方案中均观察到B试管内出现白色浑浊,则B中溶液为______(填名称) ;实验二的设计原理是_____________。 |
【题目】通过学习,我们已经了解了常见金属在溶液中的活动性顺序。铬(Cr)是重要的金属材料,越来越受到人们的关注。某化学兴趣小组对Cr、Al、Cu的金属活动性顺序进行探究,过程如下:
(提出假设)
(1)对三种金属的活动性顺序提出三种可能的假设:
a.Al>Cr>Cu b.Cr>Al>Cu c.________________
(查阅资料)该研究小组必须查阅的资料是_________(填序号)
①Cr、Al、Cu三种金属的密度②Cr能否与酸反应③Cr、Al、Cu三种金属导电性
(设计实验)
同温下,取大小相同的打磨过的金属薄片,分别投入到等体积等浓度的足量稀盐酸中,观察现象,记录如表:
金属 | Cr | Al | Cu |
与盐酸反应现象 | 气泡产生缓慢,金属逐渐溶解 | 气泡产生激烈,金属迅速溶解 | 无气泡产生,金属无变化 |
(控制实验条件)
(2)打磨三种金属的目的____________;上述实验使用等浓度的盐酸溶液的理由是___________________。
(得出结论)
(3)原假设中正确的是_______(填假设中“a”“b”或“c”).写出铬(铬与盐酸反应后显+2价)与盐酸反应的化学方程式:___________。
(结论应用)
(4)根据探究结果,写出Al丝与CuSO4溶液反应的化学方程式_______________,并写出反应的实验现象___________________。
【题目】同学们通过学习知道铜与盐酸、稀硫酸不能发生反应,但却发现化学老师用铜与浓硝酸制备出了NO2气体去做物理实验。同学们对此很感兴趣,在实验室对铜与硝酸的反应进行了探究。
实验I | 实验II | ||
实验装置 | 实验现象 | 实验装置 | 实验现象 |
| 铜片逐渐消失, 有无色气泡产生,试管中上部有红棕色气体出现;溶液由无色变为蓝色 |
| 铜片逐渐消失, 产生红棕色气体,溶液由无色变为绿色 |
(探究一)实验I中产生的无色气体是什么?
(查阅资料)
(1)硝酸(HNO3)与Cu反应生成硝酸铜和含氮元素的化合物;硝酸铜溶液呈蓝色
(2)含氮元素的某些气态物质的物理性质
NH3 | NO | NO2 | |
颜色 | 无色 | 无色 | 红棕色 |
气味 | 刺激性 | 刺激性 | |
溶解性 | 极易溶于水 | 难溶于水 | 可溶于水或硝酸 |
(3)NO2与水反应生成无色的硝酸和NO气体
(猜想与假设)无色气体可能是:①NH3 ②NO
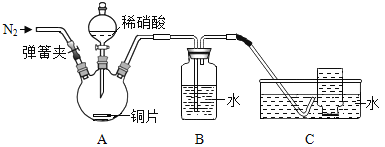
(进行实验)同学们利用下图装置对产生的无色气体进行检验。
实验操作 | 实验现象 |
1. 打开弹簧夹,通入N2,一段时间后,关闭弹簧夹 | B、C中导管口有无色气泡冒出 |
2. 将C中导管伸入集气瓶中,打开分液漏斗的活塞,滴入一定量稀硝酸,关闭活塞 | A中有无色气泡产生 B中导管口有无色气泡冒出 C中集气瓶内收集到无色气体 |
3. 从水槽中取出集气瓶,敞口置于空气中 | 无色气体变为红棕色 |
4. 取少量B中液体于试管中,滴加无色酚酞溶液 | 试管中溶液颜色无明显变化 |
(解释与结论)
(1)操作1中,通入N2的目的是_____。
(2)同学们认为猜想①不正确,理由是_____。
(3)无色气体具有的化学性质是_____。
(探究二)为什么实验II中的溶液呈绿色而不是蓝色?
(猜想与假设)①溶液中硝酸铜的质量分数较高②硝酸铜溶液中溶解了生成的气体
(设计实验)同学们设计了以下4个实验方案。
方案1 | 配制饱和硝酸铜溶液并稀释至不同的浓度,观察溶液颜色变化 |
方案2 | 加水稀释实验II所得的绿色溶液,观察溶液颜色变化 |
方案3 | 取实验II所得的绿色溶液,加热,观察溶液颜色变化 |
方案4 | 配制饱和硝酸铜溶液,…… |
(反思与评价)
(1)“方案1”和“方案3”中,能验证猜想②的是_____。
(2)“方案2”不能验证猜想①的原因是_____。
(3)“方案4”也可验证猜想②,该方案是:配制饱和硝酸铜溶液,_____。
(4)通过实验I、II与已有知识的对比,可得出的结论是_____(答一条即可)。