题目内容
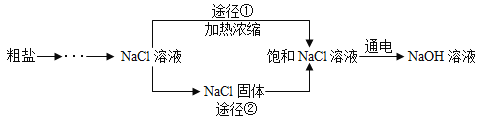
【题目】某同学设计的工业制备氢氧化钠的流程如下图。
资料:
![]() ,两电极,一端得到NaOH和
,两电极,一端得到NaOH和![]() ,另一端得到
,另一端得到![]() 。
。
(1)晾晒海水得到粗盐的原理是________________。
(2)实验室蒸发用到的仪器有铁架台(带铁圈)、坩埚钳、石棉网、酒精灯、玻璃棒和_________。
(3)工业生产中应选择途径_______(“①”或“②”),理由是_________________。
(4)![]() 可用于生产84消毒液(有效成分
可用于生产84消毒液(有效成分![]() ),反应原理为
),反应原理为![]() ,反应前后氯元素的化合价有________种。
,反应前后氯元素的化合价有________种。
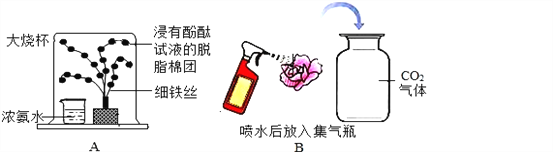
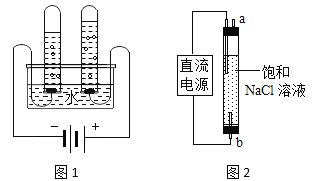
(5)图1实验测定水的组成,不能加入NaCl增强水的导电性的理由是_________。
(6)图2实验获得84消毒液,直流电源正极应与_____(填“a”或“b”)连接,才能使![]() 的含量更高。
的含量更高。
【答案】蒸发结晶 蒸发皿 ① 步骤简便,节约能源 3 会生成![]() ,干扰实验结果 b
,干扰实验结果 b
【解析】
(1)氯化钠的溶解度受温度变化影响较小,所以晾晒海水得到粗盐的原理是蒸发结晶;
(2)实验室蒸发用到的仪器还有蒸发皿;
(3)根据流程图可以看出,途径①没有将氯化钠蒸干,只是进行了浓缩,工业生产中应选择途径①,理由是途径①的步骤简便,节约能源;
(4)反应前氯气中氯元素为0价,反应后氯化钠中氯元素的化合价为-1价,反应后次氯酸钠中氯元素的化合价为+1,所以反应前后氯元素的化合价有3种。
(5)要测定水组成,不能加入NaCl增强水的导电性是因为加氯化钠会生成氯气,干扰实验结果。电解水时生成氢气和氧气,化学方程式为2H2O![]() 2H2↑+O2↑,
2H2↑+O2↑,
(6)图3实验获得84消毒液,分别在阴极与阳极生成氢气(H2)与氯气(Cl2),为了使氯气被完全吸收,直流电源正极应与b连接,才能使NaClO的含量更高。

 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案【题目】某化学兴趣小组同学,用盐酸和氢氧化钠进行“酸碱中和反应”的探究,进行一段时间后发现没有明显变化,询问老师才知道忘记滴加指示剂。因此,他们停止实验,并在老师的指导下对烧杯内的溶液中的溶质的成分进行探究。
(提出问题)该烧杯内的溶质是什么?
(猜想假设)猜想一:NaCl 猜想二:NaCl和HCl
猜想三:NaCl和NaOH 猜想四:NaCl、NaOH和HCl
同学们讨论后一致认为猜想四不合理,请你说出不合理的理由______________________(用化学方程式表示)。
(查阅资料)NaCl溶液呈中性。
(实验探究)兴趣小组甲、乙、丙三位同学分别设计了如下的实验方案,请你帮助他们完成实验报告的相关内容。
实验方案 | 实验现象 | 实验结论 |
甲同学取少量烧杯内的溶液于试管中,滴入酚酞试液 | 溶液无变化 | 猜想一成立 |
乙同学另取少量烧杯内的溶液于试管中,加入_______。 | 有气泡生成 | 猜想二成立 |
丙同学另取少量烧杯内的溶液于试管中,滴加适量的CuSO4溶液 | 没有蓝色沉淀产生 | 猜想____不成立 |
(评价反思)老师看了甲、乙、丙三位同学的实验报告,指出甲同学的实验结论不准确,请你分析甲同学实验结论不准确的原因:___________。
(得出结论)猜想二成立
(拓展延伸)某同学在进行酸碱中和滴定实验时,测得溶液的pH变化如下图1所示,请回答下列问题:

(1)由图1可知,该同学实验操作是________________。
A.将盐酸滴入氢氧化钠溶液中
B.将氢氧化钠溶液滴入盐酸中
(2)由图1可知,在b点处溶液中溶质是______________________。
(3)图2为盐酸和氢氧化钠溶液反应的微观过程,从微粒的角度分析,此反应的微观实质_______________(合理答案即可)。
【题目】我们日常生活中,食用的食盐大多来自海水晾晒.海水经蒸发结晶后可获得含有少量泥沙和杂质的粗盐.
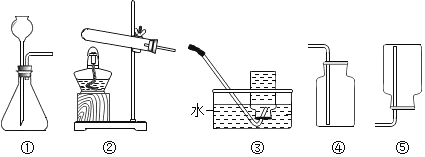
(1)为了除去粗盐中含有的少量泥沙,某小组设计了如图所示的实验:在粗盐提纯的过程中,正确的操作顺序是(填序号)______;
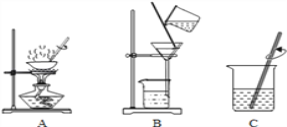
(2)准备过滤器时,为了让折好的滤纸紧贴漏斗壁,应该怎样操作:__________。
(3)实验小组实验数据如下:
称取粗盐/g | 溶解粗盐/g | 剩余粗盐/g | 精盐/g | 精盐产率/% |
5.0 | 3.6 | 1.4 | 2.8 | ? |
该同学的精盐产率为:_______ 。(保留整数)
(4)某同学所得的产率与其他同学比较明显偏低,下列哪些情况导致产率明显偏低______(选填字母序号)
A.溶解时将5.0g粗盐一次全部倒入10mL水中,立即过滤
B.蒸发时有少量液体、固体溅出
C.提纯后的精盐尚未完全干燥就称其质量
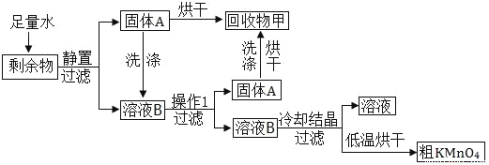
(5)粗盐提纯后得到的“精盐”中还含有少量可溶性杂质CaCl2、MgCl2.实验小组的同学设计了以下实验方案来除去可溶性杂质.
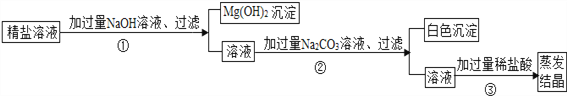
①步骤①的化学方程式为___________。
②步骤②中的白色沉淀为___________。
③步骤③中加稀盐酸是为了除去溶液中_____________。