题目内容
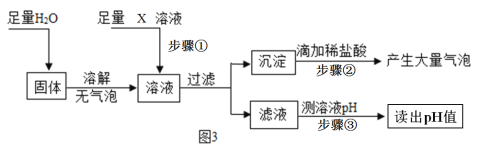
【题目】兴趣小组获得两包制作“跳跳糖”的添加剂,一包是柠檬酸晶体,另一包是标注为钠盐的白色粉末。将少量柠檬酸和这种白色粉末溶于水,混合后产生了使澄清石灰水变浑浊的气体。于是对白色粉末的化学成分进行了以下探究:
(提出猜想)猜想1.碳酸钠;猜想2.碳酸氢钠;猜想3.碳酸钠和碳酸氡钠
(查阅资料)
①碳酸钠溶液、碳酸氢钠溶液均呈碱性;
②碳酸氢钠受热分解生成碳酸钠、水和二氧化碳;碳酸钠受热不分解;
(实验探究)小月、小妮分别对有关猜想设计方案并进行实验。
实验操作 | 实验现象 | 实验结论 | |
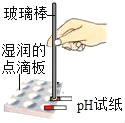
小月 | 将白色粉末溶于水后用pH试纸测定其酸碱度 | pH_____7(填“>”、“<”或“=”) | 溶液呈碱性,猜想1成立 |
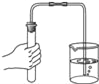
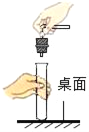
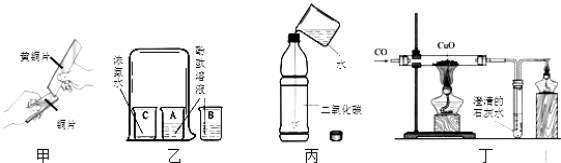
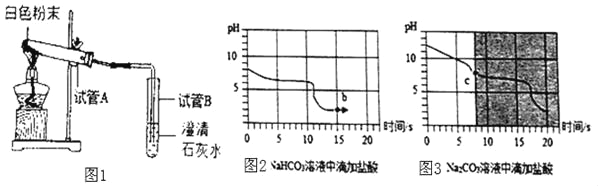
小妮 | 用如上图所示的装置进行实验 | 试管A中有水珠产生,试管B中液体变浑浊 | 猜想2成立。 |
(交流反思)大家一致认为小月和小妮的结论不准确:
(1)小月实验结论不准确的原因是__________________。
(2)小妮的实验方案不能排除白色粉末是否含有__________________。
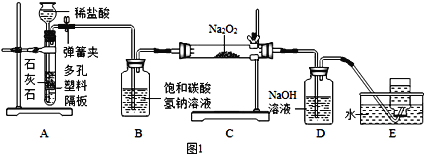
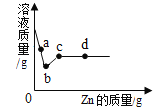
(继续探究)小戚称取mg白色粉末与足量稀盐酸反应,充分反应后生成二氧化碳的质量为ng,通过计算并分析实验数据确定猜想3正确,则n的取值范围为__________________(用含m的代数式表示)。
(结论分析)探究后他们核查到添加剂的成分是柠檬酸和碳酸氢钠,分析后认为白色粉末中的碳酸钠是由碳酸氢钠分解产生的。
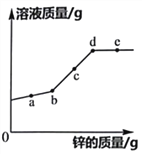
(拓展探究)向等体积、含等碳原子数的碳酸氢钠和碳酸钠溶液中,分别逐滴加入一定浓度的盐酸,得到pH变化与时间的关系如图所示。
(交流反思2)b点的溶质为__________________(写化学式),将图2和图3的阴影部分进行叠加,发现两者基本重合,C点的溶质__________________(写化学式)。
(得出结论)通过上述分析,碳酸钠和盐酸反应过程,可以依次用以下两个化学方程式表示:________、__________。
(结论与反思)探究溶液的酸碱性及反应pH值的变化,可以认识反应原理及进行的过程。
【答案】>由于碳酸钠溶液、碳酸氢钠溶液均呈碱性碳酸钠![]() NaCl、HClNaCl、NaHCO3Na2CO3+HCl=NaCl+NaHCO3NaHCO3+HCl═NaCl+H2O+CO2↑
NaCl、HClNaCl、NaHCO3Na2CO3+HCl=NaCl+NaHCO3NaHCO3+HCl═NaCl+H2O+CO2↑
【解析】
实验探究小月:根据碳酸钠溶液呈碱性分析溶液的pH;交流反思:(1)小月根据碳酸钠溶液、碳酸氢钠溶液均呈碱性分析;(2)根据碳酸钠和碳酸氢钠的混合物受热分解生成了水和二氧化碳分析;继续探究:根据碳酸钠、碳酸氢钠的化合物与与盐酸的反应分析计算;交流与反思:根据图中提供的信息可以判断相关方面的问题。
实验探究小月:由于碳酸钠溶液呈碱性。所以溶液的pH>7;交流反思:(1)由于碳酸钠溶液、碳酸氢钠溶液均呈碱性,溶液的pH>7,所以小月实验结论不准确;(2)由于碳酸钠和碳酸氢钠的混合物受热也会生成了水和二氧化碳,所以不能排除包色粉末中混有碳酸钠;
继续探究:若碳酸钠的质量为m,设与盐酸反应生成的二氧化碳的质量为x
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 44
m x
则![]() ,解得:x=
,解得:x=![]()
若碳酸氢钠的质量为m,设与盐酸反应生成的二氧化碳的质量为y。
NaHCO3+HCl═NaCl+H2O+CO2↑
84 44
m y
则![]() ,解得:y=
,解得:y=![]()
猜想3正确,即白色粉末是碳酸钠和碳酸氢钠的混合物,则n的取值范围为:![]() <n<
<n<![]() ;交流与反思2:碳酸氢钠和稀盐酸反应生成氯化钠、水和二氧化碳,b点时稀盐酸过量,因此溶质是反应生成的NaCl和过量的HCl;将图2和图3的阴影部分进行叠加,发现两者基本重合,说明向碳酸钠溶液中加入稀盐酸时,碳酸钠先和稀盐酸反应生成碳酸氢钠和氯化钠,然后碳酸氢钠再和稀盐酸反应生成氯化钠、水和二氧化碳,因此c点的溶质是反应生成的NaCl和NaHCO3;得出结论:通过上述分析,碳酸钠和盐酸反应的过程是:碳酸钠先和稀盐酸反应生成碳酸氢钠和氯化钠,然后碳酸氢钠再和稀盐酸反应生成氯化钠、水和二氧化碳,反应的化学方程式为:Na2CO3+HCl=NaCl+NaHCO3,NaHCO3+HCl═NaCl+H2O+CO2↑。
;交流与反思2:碳酸氢钠和稀盐酸反应生成氯化钠、水和二氧化碳,b点时稀盐酸过量,因此溶质是反应生成的NaCl和过量的HCl;将图2和图3的阴影部分进行叠加,发现两者基本重合,说明向碳酸钠溶液中加入稀盐酸时,碳酸钠先和稀盐酸反应生成碳酸氢钠和氯化钠,然后碳酸氢钠再和稀盐酸反应生成氯化钠、水和二氧化碳,因此c点的溶质是反应生成的NaCl和NaHCO3;得出结论:通过上述分析,碳酸钠和盐酸反应的过程是:碳酸钠先和稀盐酸反应生成碳酸氢钠和氯化钠,然后碳酸氢钠再和稀盐酸反应生成氯化钠、水和二氧化碳,反应的化学方程式为:Na2CO3+HCl=NaCl+NaHCO3,NaHCO3+HCl═NaCl+H2O+CO2↑。

【题目】在研究酸和碱的化学性质时,某小组想证明稀硫酸和氢氧化钠溶液混合后,虽然无明显现象,但确实发生了化学反应。试与他们一起完成实验方案的设计、实施和评价,并得出有关结论。
(1)探究稀硫酸和氢氧化钠溶液的反应。
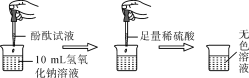
当在NaOH溶液中滴入几滴酚酞试液后,溶液由无色变为______色。根据上述实验中颜色变化,可确定稀硫酸和氢氧化钠溶液发生了化学反应,反应的化学方程式为________________。
(2)探究上述稀硫酸和氢氧化钠溶液反应后烧杯中的硫酸是否过量。
根据上述反应过程中溶液变成无色,不能确定稀硫酸是否过量。同学们又分别选取氯化钡溶液、紫色石蕊试液设计实验方案,请你判断并
实验方案 | 实验步骤 | 实验现象 | 实验结论 |
方案一 | 取样,滴入适量的氯化钡溶液 | 出现白色沉淀 | 稀硫酸过量 |
方案二 | 取样,滴入几滴紫色石蕊试液 | 溶液变红 | 稀硫酸过量 |
上述设计的实验方案中,正确的是_________(填“方案一”或“方案二”);另外一个实验方案错误的原因是__________________________。