题目内容
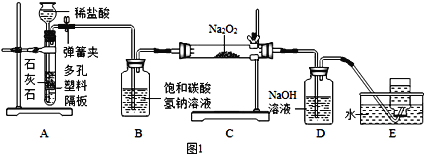
【题目】探究学习小组在实验室中用下图所示装置制取 CO2 并探究 CO2与过氧化钠( Na2O2 )的反应。
(查阅资料)过氧化钠( Na2O2 )是一种淡黄色固体,能与 CO2、H2O发生反应:2Na2O2+2CO2=2Na2CO3+O2,2Na2O2+2H2O=4NaOH+O2↑。
请回答下列问题:
(1)15.6gNa2O2固体含钠元素的质量为_____________;
(2)装置 A 中发生反应的化学方程式为_______________,利用装置 A 制取 CO2 的优点是____________;
(3)装置B的作用是______________;
(4)装置D中发生反应的化学方程式为____________________;
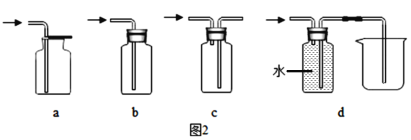
(5)装置E中收集的气体还可用下图2装置中_________________(填字母序号)收集;
(6)为探究反应后装置 C 硬质玻璃管中固体的成分,该小组同学进行了如图3实验:
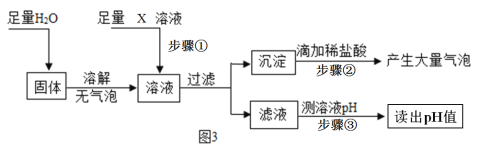
Ⅰ. 根据步骤的现象判断,反应后装置C硬质玻璃管中的固体含有________(填化学式)。
Ⅱ. 步骤①中的X溶液可能是________(填化学式)溶液,若步骤中读出的pH值______7(填“>”“<”或“=”),则说明剩余固体中含有NaOH。
【答案】9.2gCaCO3+2HCl==CaCl2+H2O+CO2↑随时控制反应的开始和停止除去气体中的HCl,防止对后面实验的干扰2NaOH+CO2=Na2CO3+H2OadNa2CO3CaCl2>
【解析】
⑴15.6g过氧化钠中钠元素的质量为:23×2÷(23×2+16×2)×15.6g=9.2g;
⑵装置A是实验室制取二氧化碳的装置,反应式为CaCO3+2HCl==CaCl2+H2O+CO2↑,利用该装置制取二氧化碳可以做到随开随始,随关随停,即可以控制反应的开始和停止;
⑶饱和碳酸氢钠溶液用于洗掉混在二氧化碳气体中的挥发出来的氯化氢气体,防止影响后面的实验;
⑷装置D中,剩余的二氧化碳气体与氢氧化钠发生反应,方程式为2NaOH+CO2=Na2CO3+H2O;
⑸装置E负责收集氧气,氧气密度大于空气,故可用向上排空气法收集,即a,也可用排水法收集,即d;
⑹Ⅰ滴加稀盐酸反应生成气体,说明存在碳酸根离子,故反应后装置C硬质玻璃管中的固体含有碳酸钠;Ⅱ固体碳酸钠加入氯化钙反应生成碳酸钙沉淀,反应后装置C硬质玻璃管中还剩有过氧化钠,与水反应生成氢氧化钠,pH>7。

【题目】兴趣小组获得两包制作“跳跳糖”的添加剂,一包是柠檬酸晶体,另一包是标注为钠盐的白色粉末。将少量柠檬酸和这种白色粉末溶于水,混合后产生了使澄清石灰水变浑浊的气体。于是对白色粉末的化学成分进行了以下探究:
(提出猜想)猜想1.碳酸钠;猜想2.碳酸氢钠;猜想3.碳酸钠和碳酸氡钠
(查阅资料)
①碳酸钠溶液、碳酸氢钠溶液均呈碱性;
②碳酸氢钠受热分解生成碳酸钠、水和二氧化碳;碳酸钠受热不分解;
(实验探究)小月、小妮分别对有关猜想设计方案并进行实验。
实验操作 | 实验现象 | 实验结论 | |
小月 | 将白色粉末溶于水后用pH试纸测定其酸碱度 | pH_____7(填“>”、“<”或“=”) | 溶液呈碱性,猜想1成立 |
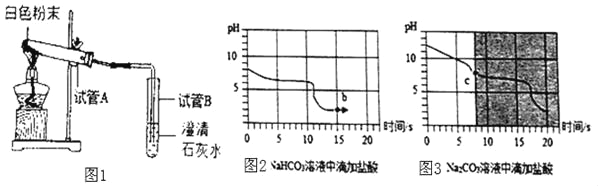
小妮 | 用如上图所示的装置进行实验 | 试管A中有水珠产生,试管B中液体变浑浊 | 猜想2成立。 |
(交流反思)大家一致认为小月和小妮的结论不准确:
(1)小月实验结论不准确的原因是__________________。
(2)小妮的实验方案不能排除白色粉末是否含有__________________。
(继续探究)小戚称取mg白色粉末与足量稀盐酸反应,充分反应后生成二氧化碳的质量为ng,通过计算并分析实验数据确定猜想3正确,则n的取值范围为__________________(用含m的代数式表示)。
(结论分析)探究后他们核查到添加剂的成分是柠檬酸和碳酸氢钠,分析后认为白色粉末中的碳酸钠是由碳酸氢钠分解产生的。
(拓展探究)向等体积、含等碳原子数的碳酸氢钠和碳酸钠溶液中,分别逐滴加入一定浓度的盐酸,得到pH变化与时间的关系如图所示。
(交流反思2)b点的溶质为__________________(写化学式),将图2和图3的阴影部分进行叠加,发现两者基本重合,C点的溶质__________________(写化学式)。
(得出结论)通过上述分析,碳酸钠和盐酸反应过程,可以依次用以下两个化学方程式表示:________、__________。
(结论与反思)探究溶液的酸碱性及反应pH值的变化,可以认识反应原理及进行的过程。