题目内容
【题目】如图是一些常见物质的转化关系,其中C是无色无刺激性的气体,且能使澄清石灰水变浑浊;E是一种无污染的清洁能源,其燃烧产物是H2O。
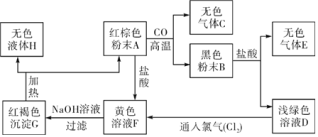
(1)红棕色粉末A、黑色粉末B和无色液体H的化学式分别为:A_____;B_____;H_____;
(2)F→G的基本反应类型是_____;
(3)A与盐酸反应的化学方程式为_____;该反应在生产生活中的一个重要用途是_____。
【答案】Fe2O3 Fe H2O 复分解反应 Fe2O3+6HCl=2FeCl3+3H2O 除铁锈
【解析】
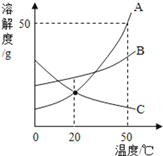
由题目对C物质的描述:无色无刺激性的气体,且能使澄清石灰水变浑浊,可确定C物质为二氧化碳;由溶液F呈黄色可判断溶液中含有Fe3+,再根据溶液F与氢氧化钠溶液反应生成红褐色沉淀G,可判断G为Fe(OH)3,根据G受热分解生成红棕色粉末A和无色液体H,可判断A为Fe2O3、H为H2O;根据A与CO高温下生成无色气体C和黑色粉末B,可判断黑色粉末为Fe;根据黑色粉末B与稀盐酸反应生成无色气体E和浅绿溶液D,可判断E为H2、溶液D为FeCl2溶液;最后根据绿色溶液D通入氯气生成黄色溶液F,可判断溶液F为FeCl3溶液,带入框图推断合理;
(1)A是一种红棕色粉末,且沉淀G受热分解可以生成A和H,可判断A为Fe2O3、H为H2O;氧化铁和一氧化碳反应可以生成无色气体C和黑色粉末B,则B可能是铁;A、B、H化学式分别为Fe2O3、Fe、H2O,故填:Fe2O3 Fe H2O;
(2)由图示可知F是氯化铁,氯化铁和氢氧化钠可以生成氢氧化铁和氯化钠,该反应的生成物产物均是化合物,且反应过程为相互交换成分,故该反应的基本类型是复分解反应,故填:复分解反应;
(3)A是氧化铁和盐酸反应的方程式为:Fe2O3+6HCl=2FeCl3+3H2O;该反应在生产生活中的一个重要用途是除铁锈,故填:Fe2O3+6HCl=2FeCl3+3H2O 除铁锈。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】下列实验操作能达到实验目的是![]()
![]()
选项 | 实验目的 | 实验操作 |
A | 检验二氧化碳中混有的少量氧气 | 将带火星的木条伸入混合气体中 |
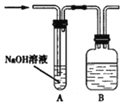
B | 除去CO2中的HCl气体 | 通入足量NaOH溶液 |
C | 除去硫酸亚铁溶液中的硫酸铜 | 加入足量的铁粉,过滤 |
D | 探究氢氧化钠溶液和稀硫酸是否恰好完全反应 | 向反应后的溶液中滴加无色酚酞试液 |
A. AB. BC. CD. D
【题目】用“盐酸——硫化钡法”生产BaCl2会放出有毒气体H2S(其水溶液有酸性),可用NaOH吸收H2S制取Na2S进行处理。下表为H2S回收工艺的各项生产成本:
表 H2S回收工艺的各项生产成本
项目 | 单价(元/吨) |
NaOH | 2500 |
Na2S | 5000 |
辅助费用(以处理1吨H2S计) | 1114 |
(1)工业处理尾气需考虑经济效益和社会效益,根据上述资料分析,单从经济效益考虑这种处理H2S的方法是______(选填“盈利”或“亏损”)的。
(2)若某化工厂每天要处理10吨H2S,需消耗NaOH多少吨__________?(写出计算过程,结果保留1位小数)