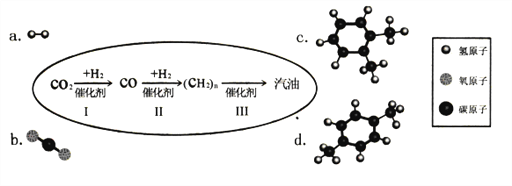
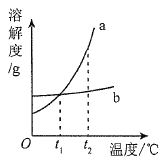
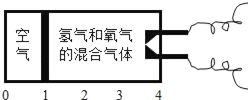
题目内容
【题目】MgSO4·7H2O是一种重要的化工原料,某工厂以一种镁矿石(主要成分为SiO2和MgCO3,还含有少量FeCO3)为原料制备MgSO4·7H2O的主要流程如下:
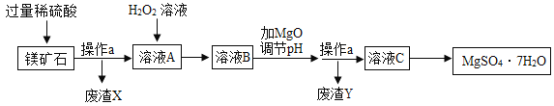
已知:SiO2既不溶于水也不溶于稀硫酸。请回答下列问题:
(1)“操作a”的名称是______。
(2)“废渣Y”中含有少量的FeOOH,其中铁元素的化合价是______。
(3)MgCO3溶于稀硫酸的化学方程式为______。
(4)“溶液A”中加入H2O2溶液会生成Fe2(SO4)3,该反应的化学方程式为______。
(5)选用MgO调节pH使Fe3+转化为沉淀,而不选用NaOH的原因是______。
【答案】过滤+3MgCO3+H2SO4=MgSO4+CO2↑+H2O2FeSO4+H2O2+H2SO4= Fe2(SO4)3+2H2O防止引入新的杂质
【解析】
(1)通过过滤可使固体与液体分离。(2)化合物中各元素化合价的代数和为零,设FeOOH中铁元素的化合价为x,则x+(-2)+(-1)=0,解得x=+3。(3)碳酸盐与稀硫酸反应生成硫酸盐、水、二氧化碳。(4)“溶液A”中含有生成的FeSO4、剩余的稀硫酸,加入H2O2溶液,发生化学反应,反应前后元素种类不变,所以反应的化学方程式为:2FeSO4+H2O2+H2SO4= Fe2(SO4)3+2H2O。(5)反应B中含有稀硫酸,MgO+H2SO4==MgSO4+H2O,因为要制备MgSO4·7H2O,该反应无杂质生成,如果加入NaOH,会引入新的杂质。

【题目】金属资源在生活中有着极其广泛的应用。
(1)铝的广泛存在及应用
①铝在地壳中的含量居所有金属元素第_____位。
②铝是很活泼的金属,但用铝制作的炊具却耐腐蚀,其原因是_____(以方程式表示)。 长期使用铝制炊具会使人体摄入过量的“铝”,不利人体健康。这里的“铝”是指_____。
a单质 b元素 c原子 d分子
③明矾中也含有铝元素,生活中用明矾净水的原理是_____。
(2)铁的冶炼:图1为某钢铁公司的矿石选取、冶铁和炼钢的工艺流程。
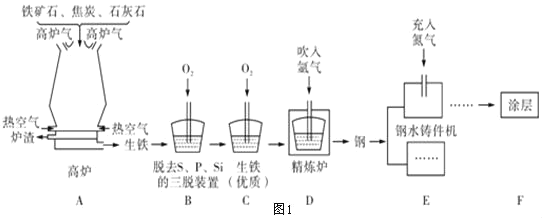
①用赤铁矿石冶铁的反应原理是_____(用化学方程式表示)。
②分析工艺流程,三脱装置中发生反应的化学方程式是_____(任写一个)。
③在钢水铸件机中,高温钢加工成钢制零件时,充入氮气的作用是_____。
(3)铁的防护:某同学为探究铁制品锈蚀的条件,进行如下实验:
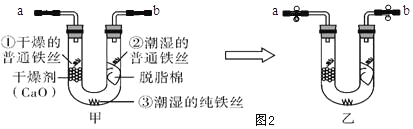
步骤 1:利用图甲所示装置,将干燥的O2从导管
a 通入U形管(装置气密性良好,药品如图甲所示);待U形管内充满O2,用止水夹夹紧导 管a、b 处连接胶皮管,如图乙所示。
步骤 2:一段时间后,观察U形管内的铁丝,其现象如表所示。
实验序号及对象 | 现象 |
①干燥的普通铁丝 | 没有明显变化 |
②潮湿的普通铁丝 | 较多红褐色锈斑 |
③潮湿的纯铁丝 | 没有明显变化 |
①步骤1中,如何证明U形管内O2已充满?_____。
②水是铁制品锈蚀的条件之一,此实验中_____(填实验序号)作对比能证明该结论。
③通过此实验还可得出影响铁制品锈蚀的因素是_____。
【题目】下列知识整理的内容不完全正确的一组是( )
A化学反应基本类型 | B化学与生活 |
①化合反应C+O2 ②解反应H2CO3=H2O+CO2↑ ③置换反应C+2CuO ④复分解反应HCl+AgNO3=AgCl↓+HNO3 | ①液氧﹣﹣可用于火箭的助燃剂 ②人体缺乏碘元素﹣导致甲状腺肿大 ③鉴别羊毛和合成纤维﹣点燃后闻气味 ④用洗洁精除去餐具油污一利用乳化作用 |
C化学实验数据记录 | D化学中常见的“三” |
①托盘天平称取7.8g铁粉 ②250mL量筒量取47.25mL水 ③用pH试纸测得苹果汁的pH为3.2 | ①煤、石油、天然气一一三大化石燃料 ②塑料、合成纤维、合成橡胶﹣﹣三大合成材料 ③分子、原子、离子一一构成物质的三种基本粒子 |
A. AB. BC. CD. D
【题目】下表所列各组物质中,物质之间按箭头方向通过一步反应就能实现如图所示转化的是( )
物质 选项 | 甲 | 乙 | 丙 | 丁 |
A | H2O | CO2 | CuO | O2 |
B | CuSO4 | H2SO4 | HCl | Fe |
C | NaCl | Na2CO3 | KNO3 | NaOH |
D | Ca(NO3)2 | CaCl2 | CaCO3 | Ca(OH)2 |
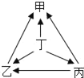
A. AB. BC. CD. D