题目内容
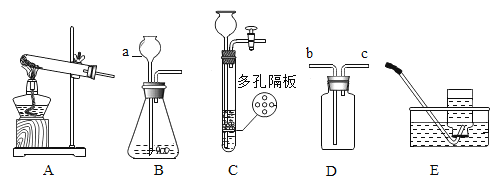
【题目】下图是实验室常用的实验装置,请回答下列问题
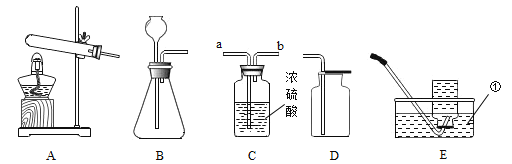
(1)仪器①的名称是 _____。
(2)实验室用 A 装置制取 O2,请写出有关化学反应方程式__________;可用 D 装置收集氧气,其原理是 _____。
(3)实验室制取并收集 CO2,选用的装置组合为 _____(填字母)。在添加药品前,应先进行的操作是_________,若用装置 C 干燥 CO2,气体由导管_________端(填“a”或“b”)通入。
(4)某学校研究小组为探究氢氧化钠与二氧化碳的反应,在室温为 15℃时,同学们将 10g 氢氧化钠固体完全溶解溶于 80g 水中,然后匀速的通入二氧化碳气体,同时用传感器测定溶液的 pH 变化,数据采集器记录并绘制的图像如下图所示。(资料链接:Na2CO3+ CO2+H2O= 2NaHCO3)
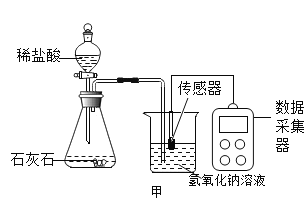
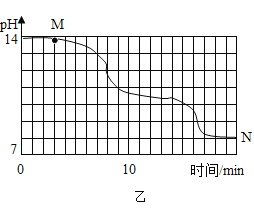
①如图甲所示实验中,用“分液漏斗”而不用“长颈漏斗”的原因是 _____;
②乙图中 M 点发生的主要化学反应方程式为 _____;
③请写出乙图 N 点对应溶液中的溶质 _____;
④上述实验能得出的结论是 _____(填序号)。
a.碳酸氢钠溶液显碱性
b.若往 NaOH 溶液不断通入 CO2 至过量,溶液最终呈酸性
c.相同浓度的 Na2CO3 溶液和 NaHCO3 溶液,碱性大小关系为:Na2CO3> NaHCO3
【答案】水槽 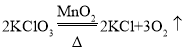 氧气密度比空气大 BD 检查装置气密性 a 分液漏斗能控制反应速率,使二氧化碳气体匀速通入 2NaOH+CO2 =Na2CO3+H2O NaHCO3 a、c
氧气密度比空气大 BD 检查装置气密性 a 分液漏斗能控制反应速率,使二氧化碳气体匀速通入 2NaOH+CO2 =Na2CO3+H2O NaHCO3 a、c
【解析】
根据实验室制气体的发生装置、收集装置的选择、实验步骤和气体的净化进行分析;读懂题目的所给信息,利用信息作答。
(1)仪器①的名称是水槽。
(2)实验室用A装置制取O2,即固体和固体反应,化学反应方程式是2KClO3 ![]() 2KCl+3O2↑;D 装置是向上排空气法收集氧气,因为氧气的密度比空气略大;
2KCl+3O2↑;D 装置是向上排空气法收集氧气,因为氧气的密度比空气略大;
(3)实验室用石灰石和稀盐酸制取CO2所以发生装置选择B,因为CO2能溶于水,密度比空气大,收集CO2应用D装置;在添加药品前,应先进行的操作是检查装置气密性,若用装置C干燥CO2,必须让二氧化碳和浓硫酸接触,气体由导管a 端通入;
(4)①如图甲所示实验中,题目要求二氧化碳要匀速通入,让反应充分,则需要控制反应速率,分液漏斗带有活塞,能够控制反应物的滴入量,从而能控制反应速率,使二氧化碳气体匀速通入;
②由乙图知M点pH开始下降,说明氢氧化钠在减少被消耗,此时二氧化碳和氢氧化钠反应生成碳酸钠和水,反应的化学方程式为:2NaOH+CO2 =Na2CO3+H2O;
③由乙图N点及以后pH图像较平稳,说明此时溶质只有一种,即碳酸钠与二氧化碳和水反应生成碳酸氢钠,所以溶质为NaHCO3;
④a.由乙图N点后溶液的溶质为NaHCO3,pH>7,说明最终溶质碳酸氢钠形成的溶液是显碱性,符合题意;
b.由乙图溶液最终pH>7说明溶液显碱性,不符合题意;
c.根据乙图象可知,碳酸钠溶液的pH在10~11之间,而碳酸氢钠溶液的pH在7~8之间,所以碳酸钠溶液的碱性大于碳酸氢钠,符合题意。故选a、c。