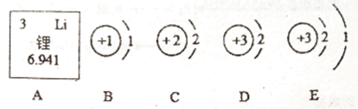题目内容
【题目】下表是部分元素的原子结构示意图、主要化合价等信息,请完成以下填空:
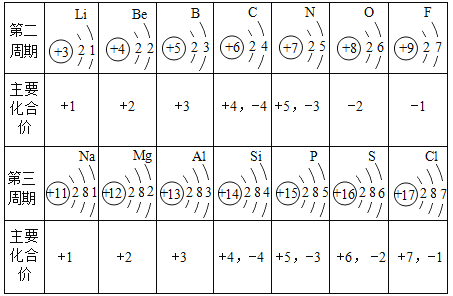
(1)原子序数为8和14的元素组成的化合物的化学式为_________。
(2)硫原子在化学反应中易____(填“得”或“失”)电子,成为____(填符号)。
(3)请你总结出此表中的原子结构与元素化合价或周期数的关系____________(任写一条)。
【答案】SiO2 得 S2- 最外层电子数=正化合价数,负化合价数=8-最外层电子数;原子结构和周期数的关系是:周期数=电子层数
【解析】
(1)8号元素是氧,容易得到两个电子而达到稳定结构,化合价为-2,14号元素是硅,能失去四个电子达到稳定结构,化合价为+4,组成化合物的化学式为SiO2;
(2)硫最外层有6个电子,在化学反应中容易得到2个电子形成稳定结构,此时为硫离子,符号为S2-;
(3)同一周期的元素,最高价态为最外层电子数(O、F除外);最外层电子数=正化合价数,负化合价数=8-最外层电子数;原子结构和周期数的关系是:周期数=电子层数;同一周期的电子层数相同。

练习册系列答案
 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案 新思维寒假作业系列答案
新思维寒假作业系列答案
相关题目