题目内容
【题目】某化学兴趣小组同学依据教材实验对化学反应前后物质的总质量变化进行了探究。
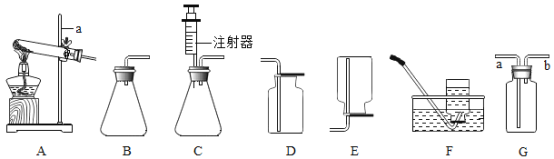
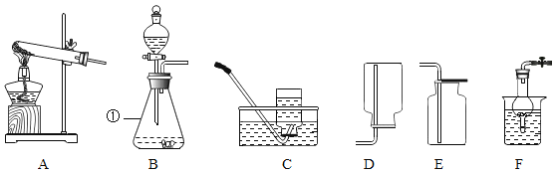
[实验装置设计]甲、乙、丙小组同学分别设计如图装置:
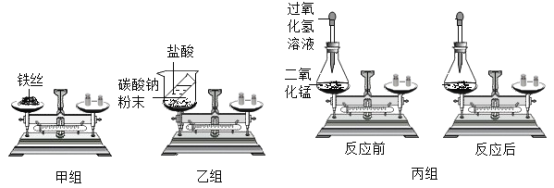
[步骤与探究](1)甲组同学取一根打磨干净的细铁丝和一个石棉网,将它们一起放在托盘天平上用砝码平衡,取下铁丝,将铁丝放在充满氧气的集气瓶中点燃,燃烧结束并冷却至室温后将所得的物质与石棉网起再放回托盘天平上称量,天平指针向左偏转。铁丝燃烧的现象是________________。
(2)乙组同学取下烧杯并将其倾斜,使物质混合发生反应,待反应后再把烧杯放到天平上,可观察到天平指针_______________ (填“ 向左偏转”、“向右偏转”或“指向中间”)。
(3)丙组同学将过氧化氢溶液挤入锥形瓶中发生反应。通过观察实验过程中天平指针的现象,得出的结论是参加化学反应的各物质的质量总和________________ (填“ 大于”、“等于”或“小于”)反应后生成的各物质的质量总和。写出装置中发生反应的化学方程式________________。
[实验分析](4)三组同学经过讨论分析,认为丙组的实验结论是正确的,请从原子的角度解释________。
[反思与交流](5)通过甲、乙、丙小组实验的探究,你得到的启示是利用有气体生成或参加的反应进行探究质量守恒定律的实验时,反应应在________________容器中进行。
【答案】剧烈燃烧,火星四射,生成黑色固体 向右偏转 等于 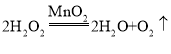 化学反应前后原子的种类不变、原子的质量不变、原子的个数不变 密闭
化学反应前后原子的种类不变、原子的质量不变、原子的个数不变 密闭
【解析】
(1)铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体。
(2)稀盐酸与碳酸钠反应生成的二氧化碳气体从烧杯逸出,所以烧杯内质量减少,天平的哪一端重,指针指向哪一端,所以向右偏转。
(3)参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和。过氧化氢溶液在二氧化锰作催化剂的条件下,发生分解反应生成水、氧气,反应的化学方程式为: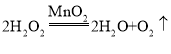
(4)发生化学反应时,分子分解为原子,原子再重新结合为新的分子,所以化学反应前后原子的种类不变、原子的质量不变、原子的个数不变。
(5)有气体生成或参加的反应进行探究质量守恒定律的实验时,反应应在密闭容器中进行。

【题目】密闭容器中有 X、氧气和二氧化碳三种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表。根据表中信息,判断下列说法正确的是 ( )
物质 | X | O2 | CO2 | H2O |
反应前质量/g | 16 | 70 | 1 | 0 |
反应后质量/g | 0 | 待测 | 45 | 36 |
A.该反应为分解反应
B.X 中一定含有碳、氢两种元素
C.表中“待测”值为 5
D.反应生成的 CO2 和 H2O 的质量比为 45:36