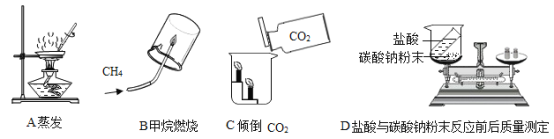
题目内容
【题目】密闭容器中盛有C2H4和O2的混合气体,点燃使其充分反应,生成CO,同时得到8.8gCO2和5.4gH2O.则参加反应的C2H4的质量为_________g;该反应的化学方程式为_____________。
【答案】4.2 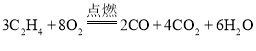
【解析】
点燃C2H4和O2的混合气体,充分反应,生成CO,得到8.8gCO2和5.4gH2O。由质量守恒定律可知:8.8gCO2中碳元素的质量为:8.8g×![]() =2.4g,CO2中氧元素的质量为:8.8g-2.4g =6.4g;5.4gH2O中氢元素的质量为:5.4g×
=2.4g,CO2中氧元素的质量为:8.8g-2.4g =6.4g;5.4gH2O中氢元素的质量为:5.4g×![]() =0.6g,5.4gH2O中氧元素的质量为:5.4g -0.6g=4.8g。氢元素全部来自于C2H4,故则参加反应的C2H4的质量为
=0.6g,5.4gH2O中氧元素的质量为:5.4g -0.6g=4.8g。氢元素全部来自于C2H4,故则参加反应的C2H4的质量为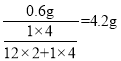 ,C2H4中碳元素的质量
,C2H4中碳元素的质量![]() ;反应前后碳元素质量不变,C2H4的碳元素质量等于一氧化碳中的碳元素和二氧化碳中的碳元素的质量之和,故一氧化碳中碳元素的质量为3.6g-2.4g=1.2g,一氧化碳的质量为
;反应前后碳元素质量不变,C2H4的碳元素质量等于一氧化碳中的碳元素和二氧化碳中的碳元素的质量之和,故一氧化碳中碳元素的质量为3.6g-2.4g=1.2g,一氧化碳的质量为 ,一氧化碳中氧元素的质量为2.8g-1.2g=1.6g;反应前后氧元素质量不变,氧气的氧元素质量等于一氧化碳中的氧元素和二氧化碳中的氧元素和水中的氧元素的质量之和,参加反应的氧气的质量=1.6g+6.4g+4.8g=12.8g;参加反应的C2H4和O2的质量比=4.2g:12.8g=21:64,而相对分子质量之比=(12×2+1×4):(16×2)=7:8;所以C2H4分子和O2分子的数量比=
,一氧化碳中氧元素的质量为2.8g-1.2g=1.6g;反应前后氧元素质量不变,氧气的氧元素质量等于一氧化碳中的氧元素和二氧化碳中的氧元素和水中的氧元素的质量之和,参加反应的氧气的质量=1.6g+6.4g+4.8g=12.8g;参加反应的C2H4和O2的质量比=4.2g:12.8g=21:64,而相对分子质量之比=(12×2+1×4):(16×2)=7:8;所以C2H4分子和O2分子的数量比=![]() =3:8。经过配平,该反应的化学方程式为
=3:8。经过配平,该反应的化学方程式为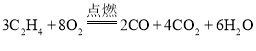 。
。

【题目】某课外活动小组的同学在整理化学药品柜时,发现一瓶标签受损的无色液体,如图所示.老师告诉大家,该瓶液体是下列5种液体中的某一种:稀H2SO4、H2O、MgCl2溶液、NaOH溶液、CuSO4溶液.
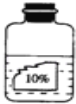
(1)根据以上信息判断,该无色液体一定不是_____和______.
(2)为确定该液体的成分,同学们设计了下列实验方案,请你一起参与同学们的探究活动.
实验操作 | 实验现象 | 实验结论 |
①取该液体适量于试管中,向其中滴加无色酚酞溶液 | 溶液颜色无变化 | 该液体不是______ |
②另取该液体适量于试管中,向其中加入锌粒 | ______ | 该液体是稀H2SO4, 不是MgCl2溶液 |
(反思交流)
(3)实验操作②中发生反应的化学方程是________.