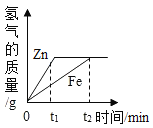
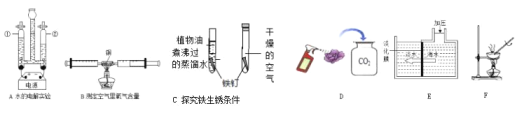
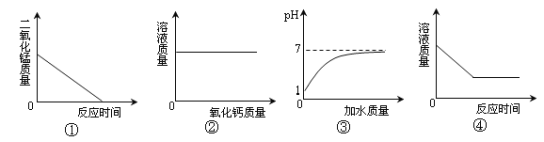
题目内容
【题目】甲、乙两种固体(不含结晶水)的溶解度曲线如图所示。下列说法正确的是 ( )
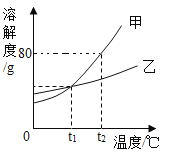
A.t1℃时,甲、乙溶液溶质的质量分数相等
B.甲中含有少量乙时,可用降温结晶法提纯甲
C.t2℃时,将 50g 甲加入 50g 水中,可以得到 100g 溶液
D.t2℃时的甲、乙饱和溶液分别降温到 t1℃时,析出晶体的质量甲大于乙
【答案】B
【解析】
A、没有确定溶液是否饱和,不能确定 t1℃时,甲、乙溶液溶质的质量分数是否相等,故A错误;
B、根据溶解度曲线可知,甲的溶解度随温度的升高变化比乙明显,故甲中含有少量的乙时,可用降温结晶法提纯甲,故B正确;
C、t2℃时,甲的溶解度为80g,根据溶解度概念可知,将50g甲加入50g水中,只能溶解40g,可得到90g溶液,故C 错误;
D,没有确定溶液的质量,不能判断t2℃时的甲、乙饱和溶液分别降温到 t1℃时,析出晶体的质量甲大于乙,故D错误。故选B。

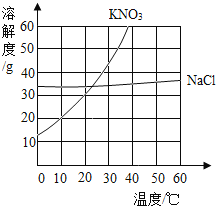
【题目】根据给出的KNO3和NaCl两种物质的溶解度表、溶解度曲线,回答问题。
温度(℃) | 0 | 20 | 40 | 60 | 80 | 100 | |
溶解度 (g/100g水) | KNO3 | 13.3 | 31.6 | 64.0 | 110.0 | 169.0 | 246.0 |
NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 | |
(1)在80℃时,NaCl的溶解度为________g;
(2)在35℃时,KNO3和NaCl两种物质中,溶解度较大的是________________;
(3)将80gKNO3、20gNaCl分别放入100g60℃的水中,充分搅拌,再到20℃,下列有关说法中,正确的是_______________。
A 0℃时有部分KNO3与溶液共存
B 降温到20℃时只有KNO3析出
C 降温到20℃时NaCl已经饱和
【题目】某矿石主要成分是 MgO,含少量的 Fe2O3、CuO 和 SiO2杂质。用该矿石制备Mg(OH)2的工艺流程简图如图:
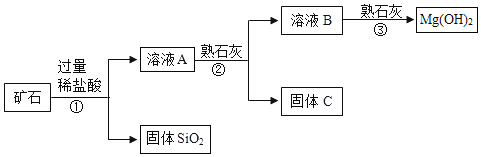
已知氢氧化铜、氢氧化铁和氢氧化镁均是沉淀,请回答下列问题:
(1)步骤①和步骤②均用到的操作是__________,需要的玻璃仪器有烧杯、漏斗和_____________。
(2)溶液 A 中所含的阳离子有 Fe3+、Cu2+、Mg2+和 __________(填离子符号)。
(3)已知部分金属阳离子以氢氧化物形成沉淀时溶液的 pH 见下表:
对应离子 | Fe3+ | Cu2+ | Mg2+ |
开始沉淀时的 pH | 1.9 | 4.2 | 9.1 |
完全沉淀时的 pH | 3.2 | 6.7 | 11.1 |
步骤②加入熟石灰,调节溶液的 pH 范围为_______________;固体 C 中所含固体成分的化学式为______________;该步骤②中所涉及的中和反应的化学方程式是______________。
(4)步骤③制取 Mg(OH)2的化学方程式为______________。
【题目】某研究性学习小组用如图所示装置进行如下实验(不考虑气体与水或盐的反应)。
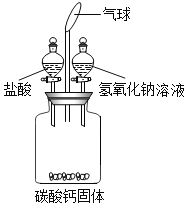
(1)先向广口瓶中加入一定量盐酸溶液,关闭活塞,震荡,观察到固体全部溶解,气球变大.然后再将一定量氢氧化钠溶液加入广口瓶中,关闭活塞,震荡,发现气球明显变小,同时在广口瓶中还能观察到的现象是_____。
(2)实验结束后,同学们对广口瓶中的溶液进行探究。
(提出问题)广口瓶中的溶液含有哪些溶质?
(交流讨论)小明取广口瓶中溶液少量加入试管内,向其广口瓶中加入过量稀盐酸,发现有气泡产生,由此他得出结论:广口瓶中溶液的溶质组成为Na2CO3、NaCl、CaCl2。大家一致认为小明的结论是错误的,理由是_____。后经大家讨论,达成共识,对广口瓶溶液中溶质组成的判断只有两种结论,结论一:_____,结论二:_____。
(实验设计)
实验步骤 | 实验现象 | 实验结论 |
①取广口瓶中溶液少量于试管中,向其中加入过量的_____溶液 | 有白色沉淀产生 | 结论一 是正确的 |
②向步骤①所得的溶液中加_____ | _____ |