题目内容
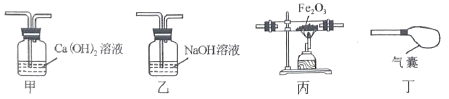
【题目】某研究性学习小组用如图所示装置进行如下实验(不考虑气体与水或盐的反应)。
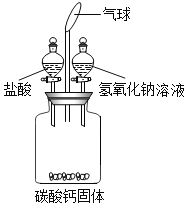
(1)先向广口瓶中加入一定量盐酸溶液,关闭活塞,震荡,观察到固体全部溶解,气球变大.然后再将一定量氢氧化钠溶液加入广口瓶中,关闭活塞,震荡,发现气球明显变小,同时在广口瓶中还能观察到的现象是_____。
(2)实验结束后,同学们对广口瓶中的溶液进行探究。
(提出问题)广口瓶中的溶液含有哪些溶质?
(交流讨论)小明取广口瓶中溶液少量加入试管内,向其广口瓶中加入过量稀盐酸,发现有气泡产生,由此他得出结论:广口瓶中溶液的溶质组成为Na2CO3、NaCl、CaCl2。大家一致认为小明的结论是错误的,理由是_____。后经大家讨论,达成共识,对广口瓶溶液中溶质组成的判断只有两种结论,结论一:_____,结论二:_____。
(实验设计)
实验步骤 | 实验现象 | 实验结论 |
①取广口瓶中溶液少量于试管中,向其中加入过量的_____溶液 | 有白色沉淀产生 | 结论一 是正确的 |
②向步骤①所得的溶液中加_____ | _____ |
【答案】有白色沉淀产生 碳酸钠能与氯化钙反应生成碳酸钙沉淀,二者不能共存 Na2CO3、NaCl NaOH、NaCl、Na2CO3 氯化钙 酚酞试液 溶液无明显颜色变化
【解析】
根据物质的性质进行分析,碳酸钙能与盐酸反应生成二氧化碳,二氧化碳能与氢氧化钠反应生成碳酸钠,生成的碳酸钠能与氯化钙反应生成碳酸钙沉淀和氯化钠,物质间反应时存在物质过量的情况,要检验碳酸钠的存在可以采用加酸化气的方法或加入可溶性钙的化合物生成沉淀的方法。
(1)碳酸钙能与盐酸反应生成氯化钙和二氧化碳,加入氢氧化钠溶液后,氢氧化钠会与二氧化碳反应生成碳酸钠和水,生成的碳酸钠能与氯化钙反应生成碳酸钙沉淀,所以会有白色沉淀生成,所以本题答案为:有白色沉淀产生;
(2)交流讨论:碳酸钠能与氯化钙反应生成碳酸钙沉淀和氯化钠,故碳酸钠和氯化钙不会同时存在,一定会有氯化钠存在,碳酸钠与氯化钙反应时,可能是碳酸钠剩余,也可能是氯化钙剩余,小明取广口瓶中溶液少量加入试管内,向其中加入过量稀盐酸,发现有气泡产生,碳酸钠可以和稀盐酸反应生成二氧化碳和水,所以溶液碳酸钠过量,氢氧化钠和二氧化碳反应生成碳酸钠和水,氢氧化钠可能恰好完全反应,也可能有剩余。本题答案为:碳酸钠能与氯化钙反应生成碳酸钙沉淀,二者不能共存;Na2CO3、NaCl;NaOH、NaCl、Na2CO3;
实验设计:要检验碳酸钠的存在,可以使用加入可溶性钙的化合物的方法观察是否生成白色沉淀,也可以加入盐酸观察是否生成气体的方法,所以本题答案为:
验步骤 | 实验现象 | 实验结论 |
①取广口瓶中溶液少量于试管中,向其中加入过量的 氯化钙溶液 | 有白色沉淀产生 | 结论一 是正确的 |
②向步骤①所得的溶液中加 酚酞试液 | 溶液无明显颜色变化 |

 全能测控一本好卷系列答案
全能测控一本好卷系列答案【题目】Cu–Zn合金可用于工艺品的制作。某化学兴趣小组的同学为了测定某铜锌合金样品的组成,取20克样品于烧杯中,向其中分5次加入相同质量分数的稀硫酸,使之充分反应,每次所用稀硫酸的质量均为20 g,剩余固体的质量记录于下表:
实验次数 | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 |
反应后剩余固体的质量(g) | 17.4 | 14.8 | 12.2 | 10.8 | 10.8 |
试回答下列问题:
(1)Cu–Zn合金属于___________材料(“金属”或“有机合成”)。
(2)计算Cu–Zn合金完全反应时生成氢气的质量___________。(计算结果保留2位小数)