��Ŀ����
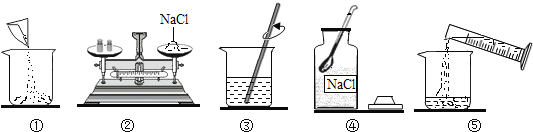
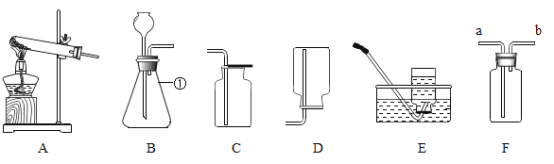
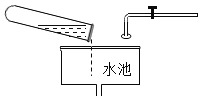
����Ŀ��ijУ��ѧ�С���ͬѧ��ѧϰ���ᡢ��εĻ�ѧ���ʺ�������ͼ1��ʾ��ʵ�飬�����������������ǵ�̽��������ش��������⡣
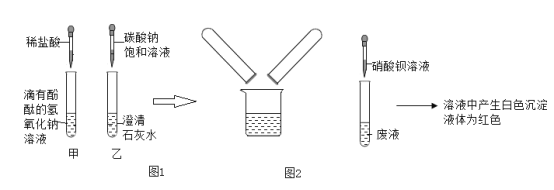
[ʵ��̽��]��ͬѧ�۲쵽��ɫ��Һ��dz���Ӷ��ó�ϡ���������������Ʒ�����Ӧ����ͬѧ��ͬ��Ĺ۵㣬������_____��ʵ�������ͬѧ�ǽ��ס��������Թ��ڵ�����ȫ������ͬһ���ɾ��ķ�Һ���У����տ����ձ���Һ����Dz��ʺ�ɫ�����˺�÷�Һ���ɴ�����ó��˷�Һ��һ�������е�������_____�������ӷ��ţ���
[�������]��Һ�г���Na+��C1���⣬������Щ�����أ�����̪���⣩
[���������]ͬѧ��˼�������������²��룺�ף�CO32��OH���ң�CO32������OH����������д��һ�ֺ������룺_____��
[���̽��]��ͬѧ��������ͼ2ʵ��
[ʵ�������]���Ǽ�ͬѧ�ó��Լ��IJ�����ȷ��С��ͬѧ�����۵ó���ͬѧ��ʵ��ó��Ľ��۲���ȷ�������ǣ�_____��С��ͬѧ�������۰Ѽ�ͬѧ��ʵ������˸Ľ������յó��˼�ͬѧ�IJ�����ȷ��
[����̽��]С��ͬѧͨ��ʵ��̽�����˷�Һ�п��ܴ��ڵ����������ӵĴ��ڣ�ͬѧ��ͨ��ʵ����֤������һ��һ�����������ӣ�ʵ�鲽�裺����ȡ��Һ������_____��Һ��Ȼ���ټ���_____��Һ�����۲쵽_____������ȷ�������ӵijɷ֡�
[��˼�����]��̽�����ӳɷ�ʱѡ���Լ�ʱҪע��������ǣ�_____��
���𰸡������Ǽ���ϡ��������Һϡ�� H+ Ca2+��OH�� ��������ᱵ��Һû��˵����������̼���Ʒ�Ӧʱ��̼���ƿ�����ʣ�̼࣬������Һ�ʼ��ԣ�Ҳ��ʹ��ɫ��̪��Һ��죬��ȷ��OH���Ƿ���� ����ϡ���� ������ ��Һ�в�����ɫ���� �Լ���������������Լ�ֻ�����������ӷ�Ӧ�������Ե�����
��������
[ʵ��̽��]
�������Һ��ϡҲ��ʹ��ɫ��Һ��dz�����ס��������Թ��ڵ�����ȫ������ͬһ���ɾ��ķ�Һ���У����տ����ձ���Һ����Dz��ʺ�ɫ��˵����Һ�Լ��ԣ�һ�����������ӣ�
[���������]
�����Ӧ���������ƹ�������Һ�л���Ca2+��OH����
[ʵ�������]
��������ᱵ��Һû��˵����������̼���Ʒ�Ӧʱ��̼���ƿ�����ʣ�̼࣬������Һ�ʼ��ԣ�Ҳ��ʹ��ɫ��̪��Һ��죬��ȷ��OH���Ƿ���ڣ�
[����̽��]
Ҫ֤�������ӵĴ���Ҫ���ų�̼������ӵĸ��ţ���������ȡ��Һ����������ϡ������Һ��Ȼ���ټ�����������Һ�����۲쵽��Һ�в�����ɫ����������ȷ�������ӵĴ��ڣ�
[��˼�����]
��̽�����ӳɷ�ʱѡ���Լ�ʱҪע���Լ����������Լ������Լ�ֻ�����������ӷ�Ӧ�������Ե�����