题目内容
【题目】小明同学为了测定用于实验室制取二氧化碳的原料石灰石(主要成分是碳酸钙)中碳酸钙的质量分数,称取11.1 g研碎的石灰石粉末样品进行四次高温加热、冷却、称量,记录数据如下(杂质不反应):
操作次序 | 第一次 | 第二次 | 第三次 | 第四次 |
剩余固体/g | 8.5 | 7.9 | 6.7 | 6.7 |
已知碳酸钙高温下分解生成氧化钙和二氧化碳,问:
(1)到第________次反应时,碳酸钙完全反应。
(2)样品完全反应时生成二氧化碳_____ g。
(3)样品中碳酸钙的质量分数是多少?(计算结果精确到0.1%)
【答案】(1)三(2)4.4(3)90.1%
【解析】
(1)由图表可知,第三次和第四次剩余固体的质量相等,说明,第三次反应已是完全反应;
(2)完全反应后生成二氧化碳的质量为:11.1g-6.7g=4.4g;
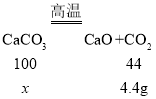
(3)设样品中碳酸钙的质量为x,
![]()
x=10g,
则样品中碳酸钙的质量分数=![]()
![]() 100%=90.1%。
100%=90.1%。

练习册系列答案
 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案
相关题目