题目内容
【题目】学习化学后,我们可以用所学的化学知识回答生活中与化学相关的问题。
(1)目前部分农村的饮用水主要还是地下水。饮用遭到污染或硬度大的地下水不利于人体健康。
① 检验某地下水是硬水还是软水,可用的物质是_________。
② 测定地下水的酸碱度可用_________。(填标号)
A.紫色石蕊溶液 B.无色酚酞溶液 C.pH试纸
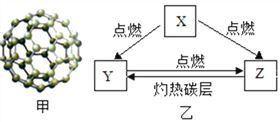
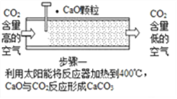
③ 自来水生产过程中,可用沉降、_________方法除去水中不溶性杂质,同时还必须进行消毒。X是一种新型的自来水消毒剂,工业上制取X 的化学方程式为:Cl2 + 2NaClO2 == 2NaCl + 2X,则X的化学式为________。
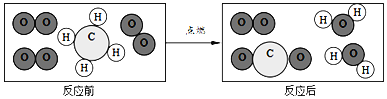
(2)现在,我们家里厨房做饭用的主要燃料为天然气,天然气的主要成分是_________(填化学式),其燃烧的化学方程式为____________,家用燃料经过了如下的更新过程
![]()
下列有关家用燃料更新的理由,正确的是_________________。
A.天然气是新能源,取之不尽用之不竭 B.气体燃料的利用率更高 C.减少煤燃烧过程中产生的污染物
【答案】肥皂水 C 过滤 ClO2 CH4 CH4+2O2![]() 2H2O+CO2 BC
2H2O+CO2 BC
【解析】
(1)①用肥皂水可检验某地下水是硬水还是软水,其中泡沫多的是软水,泡沫少的是硬水;②测定地下水的酸碱度用pH试纸,而紫色石蕊试液、无色酚酞试液只能测定溶液的酸碱性。③过滤是除去水中不溶性杂质的一种方法;根据质量守恒定律,在化学方程式为:Cl2+2NaClO2═2NaCl+2X中反应前氯原子有4个,钠原子有2个,氧原子有4个,而反应后氯化钠中钠原子有2个,氯原子有2个,所以2X中应有2个氯原子,4个氧原子,所以X的化学式为ClO2;
(2)天然气的主要成分是甲烷,甲烷燃烧产生了二氧化碳和水,该反应的化学方程式为:CH4+2O2![]() 2H2O+CO2;
2H2O+CO2;
A、天然气是不可再生的能源,不是取之不尽的,故A说法不正确;
B、气体燃料燃烧充分,利用率更高,故B说法正确;
C、气体燃料燃烧充分,产生的一氧化碳和烟尘少,减少煤燃烧过程中产生的污染物,故C说法正确。

 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案【题目】为探究碳还原氧化铜的最佳实验条件,用木炭粉和氧化铜的干燥混合物1~2.5 g进行系列实验。
(查阅资料)
①氧化铜(CuO)为黑色固体。铜不与稀硫酸反应。
②碳还原氧化铜得到的铜中可能含有少量的氧化亚铜;氧化亚铜为红色固体,能与稀硫酸反应:Cu2O + H2SO4 ==== CuSO4 + Cu + H2O
(进行实验)
实验1:取质量比为1:11的木炭粉和氧化铜混合物1.3 g,进行实验。
序号 | 1-1 | 1-2 |
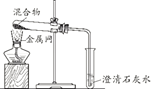
装置 |
|
|
反应后物质的颜色、状态 | 黑色粉末中混有少量红色固体 | 红色固体有金属光泽,混有极少量黑色物质 |
实验2:取一定质量的混合物,用1-2装置进行实验。
序号 | 木炭粉与氧化铜的质量比 | 反应后物质的颜色、状态 | |
2-1 | 1:9 | 红色固体有金属光泽 | 混有少量黑色物质 |
2-2 | 1:10 | 混有很少量黑色物质 | |
2-3 | 1:11 | 混有极少量黑色物质 | |
2-4 | 1:12 | 无黑色物质 | |
2-5 | 1:13 | 混有较多黑色物质 | |
(解释与结论)
(1)配平化学方程式:___C +__CuO![]() __Cu +__CO2↑
__Cu +__CO2↑
(2)实验1-2中,证明产生了CO2的现象是_______。
(3)实验1的目的是_______。
(4)实验2的结论是_______。
(反思与评价)
(5)实验2没有进行质量比为1:14的实验,理由是_______。
(6)为检验2-4的红色固体中是否含Cu2O,所需试剂是_______。
【题目】下列关于化学实验的“目的-操作-现象-结论”的描述正确的是( )
实验目的 | 操作 | 实验现象 | 实验结论 | |
A | 检验稀盐酸和氢氧化钠溶液是否恰好完全反应 | 在反应后的溶液中滴加无色酚酞试液 | 无明显现象 | 恰好完全反应 |
B | 判断海水和蒸馏水 | 蒸发结晶 | 液体消失,无残留物 | 该液体为蒸馏水 |
C | 检验溶液中是否含硫酸根离子 | 加入氯化钡溶液,再加入稀硝酸 | 有白色沉淀产生 | 溶液中一定含硫酸根离子 |
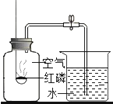
D | 测定空气中氧气的体积分数 |
| 红磷燃烧,产生大量白色烟雾;完全燃烧后,立即打开弹簧夹,进入水的体积约为集气瓶总体积的五分之一 | 氧气约占空气体积的五分之一 |
A. A B. B C. C D. D