��Ŀ����
����Ŀ����.������֪����֪�����ǻ�ѧѧϰ���õ�˼ά������ij�ܱ����������ʱ仯���̵���ʾ��ͼ����.

��ش�
�仯���ʾ�Ļ�ѧ����ʽ��______��
�仯��۲쵽�ĺ��������______��
��.�����Ǽ���Ԫ�ص�ԭ�ӽṹʾ��ͼ����ش��������⣺

��1����֪�ƺ�������Ӧ�������Ȼ��Ƶ��۱���ԭ���ǣ��γ��˴��෴��ɵ�������������õĽ�����ָ���þ�����ԭ�ӽṹʾ��ͼ�����Ʋⵥ��þ�͵�����__����������������������������Ӧ������þ��MgS��������۽Ƕ�˵�����Ʋ��������___��������ͨ��ʵ����֤�÷�Ӧ�ܷ�����
��2�����Ӣ���ij����Ԫ�ص�ԭ�ӣ�����������Ϊ���b����ͼ��X=_____���仯ѧ�����������ƣ�ԭ����___���������b�Ľ������Ա���ǿ�����ж��b�Ļ�ѧ����Ԥ���������______������ĸ����
A �b�ڸ����²�����������Ӧ
B �b����������ͭ��Һ������Ӧ
C �b����ϡ���ᷢ���û���Ӧ
���𰸡�2H2 + O2 ![]() 2 H2O �����ڱ���СҺ�Σ�Сˮ�飩���ֻ������ڱ��б��������顢���壩���� �� �����������ĵ�ʧ 3 ������������ͬ C
2 H2O �����ڱ���СҺ�Σ�Сˮ�飩���ֻ������ڱ��б��������顢���壩���� �� �����������ĵ�ʧ 3 ������������ͬ C
��������
�������ܱ����������ʱ仯���̵���ʾ��ͼ��֪���÷�Ӧ������ȼ��������ˮ���ų��������ȣ�ˮ����������������Һ̬��ˮ�����ԣ��仯���ʾ�Ļ�ѧ����ʽ��2H2 + O2 ![]() 2 H2O���仯��۲쵽�ĺ�������ǣ������ڱ���СҺ�Σ�Сˮ�飩���ֻ������ڱ��б��������顢���壩���֣��ʴ�Ϊ��2H2 + O2
2 H2O���仯��۲쵽�ĺ�������ǣ������ڱ���СҺ�Σ�Сˮ�飩���ֻ������ڱ��б��������顢���壩���֣��ʴ�Ϊ��2H2 + O2 ![]() 2 H2O�������ڱ���СҺ�Σ�Сˮ�飩���ֻ������ڱ��б��������顢���壩���֣�
2 H2O�������ڱ���СҺ�Σ�Сˮ�飩���ֻ������ڱ��б��������顢���壩���֣�
������1������ԭ�ӵ�������������Ϊ�ǽ���Ԫ�أ��õ������γ������ӣ�þΪ����Ԫ�أ���ʧ�����γ������ӣ���������������γ���þ���ʴ�Ϊ���ܣ������������ĵ�ʧ��
��2����������=�����������Ϊԭ�ӣ���113=2+8+18+32+32+18+x��x=3��
Ԫ�صĻ�ѧ���ʸ�����ԭ�ӵ�����������Ŀ��ϵ�dz����У�����Ԫ�ػ�ѧ���ʵ����������������bԪ������Ԫ�ص�ԭ��������������ͬ���bԪ������Ԫ�صĻ�ѧ�������ƣ�
A���������b�Ľ�������Ա���ǿ���b�ڳ�����Ҳ����������Ӧ����A����
B���b��ͭ���ã���������ͭ��Һ������Ӧ����B����
C���b�������ǰ�棬����ϡ���ᷢ���û���Ӧ����C��ȷ��
�ʴ�Ϊ��3��������������ͬ��C��

����Ŀ��С���������������Һʱ�õ��±����ݣ��ݴ˷�������˵����ȷ���ǣ�������
��� | �¶�/�� | ˮ������/�� | ��������ص�����/�� | ������Һ������/�� |
�� | 10 | 100 | 40 | 120.9 |
�� | 60 | 100 | 40 | 140 |
A.10��ʱ����ص��ܽ��Ϊ40��
B.��������Һһ����60��ʱ����صı�����Һ
C.��ͨ�����Ƚ�����ʣ�������ȫ���ܽ⣬����Һ�������������������ǰ����һ��
D.������������Һ������10�棬����Һ�����������������С
����Ŀ�����Ļ�ѧ���ʱȽϻ��ã������������ᡢCuSO4��Һ�ȶ������ʷ�����ѧ��Ӧ����ѧ��ȤС���ڿ��������з��֣�����Fe2O3�ڸ��������¾�ȻҲ�ܷ�����ѧ��Ӧ��
��������⣩
����Fe2O3��Ӧ�IJ�����ʲô��
���������ϣ�
��FeO��Fe2O3��Fe3O4�У�Fe2O3�Ǻ���ɫ�������Ǻ�ɫ��FeO�ڿ����л�ܿ챻������Fe2O3��Fe3O4�д��ԡ��ڶ�����̼�������÷�Ӧ�ı������������������ﶼ��������Һ��Ӧ��
����������裩
���������غ㶨�ɣ������������Fe2O3��Ӧ�IJ��
����FeO����ֻ��Fe3O4����__________��
������ʵ�飩
��1������ͼװ��ҩƷ(���۹���)����������(װ��ҩƷǰ�Ѽ��װ�õ�������)��
��2������ע��������ͨ�������̼�����Ʋ����������________��ֹͣͨ�������̼��
��3����ȼ�ƾ���Ƽ���ҩƷ���ȵ������ĩȫ����ڣ���Ϩ��ƾ���ơ�
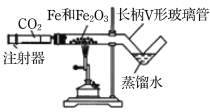
��4��������V�β�������ȴ������ʱ�������ɫ��ĩ�ɷ֡������������(����д�����еĿհ�)��
������������� | ������ | |
a | ��ɫ��ĩ��¶�ڿ����в��仯 | ��ɫ��ĩ��һ��û��___________ |
b | �ô�����������ɫ��ĩ����ȫ������ | ��ɫ��ĩ��һ����������_______ |
c | ȡ�����ĺ�ɫ��ĩװ���Թܣ��μ�������___________��Һ�����ֺ�ɫ���壬��ַ�Ӧ���Բ���������ɫ��ĩ | ȷ�ϲ���_______��ȷ |
��̽�����ۣ�
����Fe2O3�ܷ������Ϸ�Ӧ���йصĻ�ѧ����ʽ��________________��
����˼���ۣ�
��ʵ���еı������������ö�����̼���壬Ҳ����________________��
����Ŀ��ijͬѧ������¼���ʵ�飬̽��ijЩ�ᡢ���֮��ĸ��ֽⷴӦ�ܷ�����
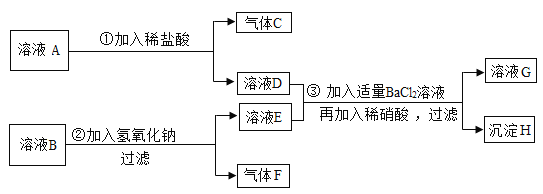
��֪��BaSO4�ǰ�ɫ���壬������ˮ��Ҳ�������ᷴӦ��
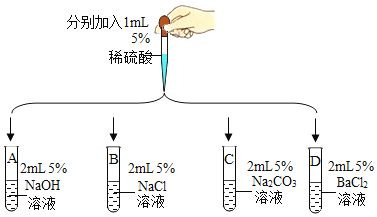
����һ�飩ѡȡ5����Һ����ͼ��ʾ����ʵ�顣
ʵ�� | ������ | ���� |
| �Թ�A��B��������������ȷ����Ӧ�Ƿ����� | / |
��1���Թ�C�в���_____����ʵ���������ֽⷴӦ�ѷ����� | ��2���Թ�C�м��ٵ�����_____ ���������ţ� | |
�Թ�D���а�ɫ�������������ֽⷴӦ�ѷ����� | ��3����Ӧ�Ļ�ѧ����ʽΪ_____ |
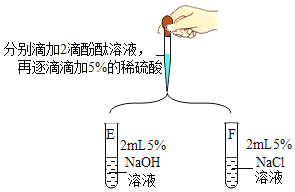
���ڶ��飩���Թ�A��B���Ƿ�����Ӧ��̽������ͼ��ʾ����ʵ�顣
ʵ�� | ������ | ���� |
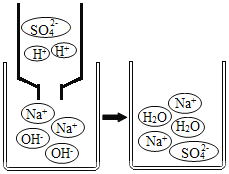
| �Թ�E�У��μӷ�̪��Һ����Һ����ɫ��Ϊ��ɫ���μ�һ����ϡ�������Һ�ɺ�ɫ��Ϊ��ɫ�����ֽⷴӦ�ѷ����� |
��4���������ӱ仯�ĽǶȷ����Թ�E�з�Ӧ��ʵ����_____�� |
�Թ�F��ʼ��������������ȷ����Ӧ�Ƿ����� |
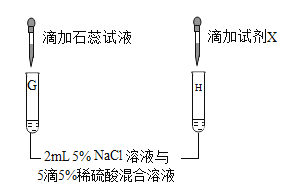
�������飩���Թ�B���Ƿ�����Ӧ����̽������ͼ��ʾ����ʵ�顣
ʵ�� | ������ | ���� |
| �Թ�G����Һ��� | ��5����ʵ���Ŀ����Ϊ�˼����Թ�G����Һ�д���_____���������ţ��� |
��6�����Թ�H�еμ�_____����Լ�X���Ļ�ѧʽ����Һ���а�ɫ���������� | ��Һ����SO42�����ڡ� | |
���� | NaCl��Һ��ϡ����������ֽⷴӦ�� | |