题目内容
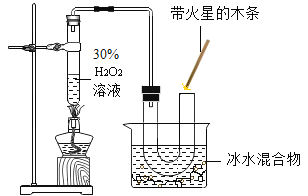
【题目】证据推理是科学研究的基本方法,已知某溶液A中的溶质可能含有Na2SO4和Na2CO3或两者之一,另有一种溶液B,其中的溶质可能是CuCl2和NH4Cl或两者之一。
按图示进行探究实验,出现的现象如图所示(设过程中所有可能发生的反应均恰好完全反应)。
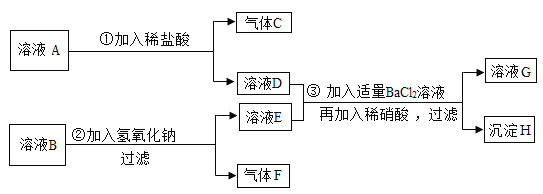
试根据实验过程和发生的现象,填写以下空白:
(1)气体C的化学式为_______,沉淀F的颜色为____。
(2)写出步骤①中发生反应的一个化学方程式___。
(3)取少量溶液G蒸发结晶,所得的固体为__(填写化学式)。
(4)由上述实验可分析出溶液A的组成为_____。
(5)由上述实验可分析出溶液B的组成为_____。
【答案】CO2 蓝色 2HCl+Na2CO3=2NaCl+CO2↑+H2O NaCl Na2SO4和Na2CO3 CuCl2
【解析】
根据碳酸根离子和氢离子反应会生成二氧化碳气体,铜离子和氢氧根离子反应会生成沉淀,铵根离子和氢氧根离子反应生成氨气,硫酸根离子和钡离子反应会生成不溶于酸的硫酸钡沉淀等知识进行分析。
碳酸根离子和氢离子反应会生成二氧化碳气体,铜离子和氢氧根离子反应会生成沉淀,铵根离子和氢氧根离子反应生成氨气,硫酸根离子和钡离子反应会生成不溶于酸的硫酸钡沉淀。溶液A加入稀盐酸产生气体C和溶液D,说明A中一定含有碳酸钠。溶液B中加氢氧化钠溶液得到溶液E和沉淀F,说明B中不含铵根离子、含有铜离子,溶液E和溶液D的混合物中加入氯化钡溶液,产生沉淀H和溶液G,说明H是硫酸钡,溶液D或E中一定含有硫酸根离子,所以A中一定含有硫酸钠。
(1)气体C为碳酸钠和盐酸反应生成的二氧化碳,化学式为CO2;
沉淀F为氯化铜和氢氧化钠反应生成的氢氧化铜,颜色为蓝色
(2)步骤①中发生的反应为碳酸钠与稀盐酸反应生成氯化钠、二氧化碳和水,该反应的化学方程式为:2HCl+Na2CO3=2NaCl+CO2↑+H2O
(3)由分析可知,溶液E中溶质为氯化钠,溶液D中离子为钠离子、硫酸根离子、氯离子,溶液D、E混合液中加氯化钡恰好完全反应,得出的滤液G溶质为氯化钠,经蒸发结晶,所得固体为NaCl
(4)由上述实验可分析出溶液A的组成为Na2SO4和Na2CO3
(5)由上述实验可分析出溶液B的组成为CuCl2

 阅读快车系列答案
阅读快车系列答案【题目】现有某纯净物X,将其配成无色溶液,取该溶液三等份,分别加入到足量的稀硫酸、澄清石灰水和氯化钠溶液中并振荡,产生的现象如下表。则有关该物质X的描述中正确的是
加入物质 | 稀硫酸 | 澄清石灰水 | 氯化钠溶液 |
实验现象 | 生成气体 | 生成沉淀 | 无明显现象 |
A.物质X中可能含有钾元素
B.物质X的溶液中可能含有SO![]()
C.物质X可能是碳酸钠
D.物质X一定是化合物