题目内容
某课外小组同学将100 g盐酸分5次加入到30g石灰石样品中( 样品中杂质既不溶于水也不与盐酸反应),得到如下部分数据和图像:
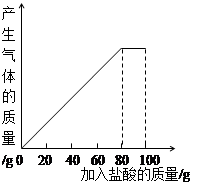
(1)从上表数据分析,第2次加入盐酸后,a为________________g;
(2)30g石灰石样品与100g稀盐酸反应共生成二氧化碳 g;
(3)求第5次实验后过滤,所得CaCl2的溶质质量分数为多少?(精确到1%)
(4)10%的CaCl2溶液可作路面保湿剂,欲将第5次实验后的溶液配成10%的CaCl2溶液,要加入水多少克?
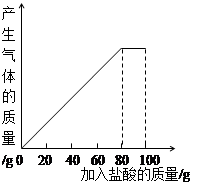
| 次数 | 第一次 | 第二次 | 第三次 |
| 加入盐酸的质量/g | 20 | 20 | 20 |
| 剩余固体的质量/g | 25 | a | 15 |
(2)30g石灰石样品与100g稀盐酸反应共生成二氧化碳 g;
(3)求第5次实验后过滤,所得CaCl2的溶质质量分数为多少?(精确到1%)
(4)10%的CaCl2溶液可作路面保湿剂,欲将第5次实验后的溶液配成10%的CaCl2溶液,要加入水多少克?
⑴20;⑵8.8g;⑶ 20%;⑷要加入水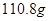 。
。
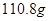 。
。试题分析:(1)由题可知,第一次加入盐酸不足量,第二次加入也不足量,所以第二次固体质量也减小5g,剩余固体的质量为20g;(2)由题可知加入稀盐酸80g时反应恰好进行完全,因此加入80g稀盐酸时产生的气体质量为30g石灰石样品与100g稀盐酸反应共生成二氧化碳的总质量,第一次加入20g稀盐酸时固体减少5g,设此时生成气体的质量为
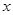 g,则有
g,则有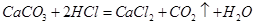
100 44
5g
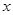
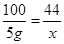 ,解得
,解得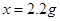 ,所以30g石灰石样品与100g稀盐酸反应共生成二氧化碳的质量为
,所以30g石灰石样品与100g稀盐酸反应共生成二氧化碳的质量为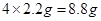 ;
;(3)设第5次实验后过滤,所得CaCl2的溶质的质量为
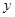 ,则有
,则有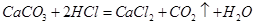
111 44
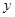 8.8g
8.8g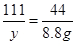 ,解得
,解得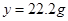
100g稀盐酸消耗的碳酸钙的总质量为
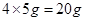
所得CaCl2的溶液总质量为:

所得CaCl2的溶液的溶质质量为
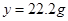
所以第5次实验后过滤,所得CaCl2的溶质质量分数为:
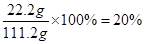 ;
;(4)设要加入水的质量为
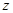 g,根据稀释前后溶质质量守恒的原则有:
g,根据稀释前后溶质质量守恒的原则有: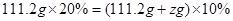
解得
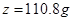 ,所以要加入水
,所以要加入水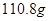 。
。点评:这是化学反应联系方程式的计算题,这种题目是每年中考的压轴题,必考题,这类题目的难点在于把坐标曲线表示的意义和题干联系起来。

练习册系列答案
相关题目

 2Fe + 3CO2
2Fe + 3CO2